
【题目】H2A为二元弱酸,常温下,向一定体积的0.1 mol·L-1的H2A溶液中逐滴加入一定浓度的NaOH溶液,溶液中不同形态的粒子(H2A、HA-、A2- )的物质的量分数a(X)随pH的变化曲线如图所示,![]()
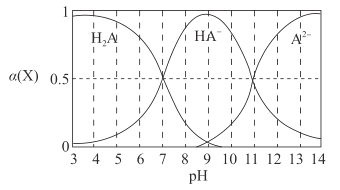
下列说法错误的是
A.K1(H2A)=1.0×10 -7B.K2(H2A)=1.0×10-11
C.pH=9时,c(Na+ )<c(HA- )+ 2c(H2A)D.pH=7时,c(Na+ )=c(H2A)+2c(A2- )
【答案】C
【解析】
A. 电离平衡常数只受温度的影响,与浓度大小无关,Ka1=![]() ,由图可知,当pH=7时,c(H2A)=c(HA-),Ka1=c(H+)=10-7,故A说法正确;
,由图可知,当pH=7时,c(H2A)=c(HA-),Ka1=c(H+)=10-7,故A说法正确;
B. 根据A选项分析,pH=11时,c(A2-)=c(HA-),Ka2=c(H+)=10-11,故B说法正确;
C. 根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),pH=9的溶液显碱性,c(H+)<c(OH-),即c(Na+)>c(HA-)+2c(A2-),由图像可知,pH=9时, c(A2-)=c(H2A),代入表达式,c(Na+)>c(HA-)+2c(H2A),故C说法错误;
D. 根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),pH=7时,c(H+)=c(OH-),c(H2A)=c(HA-),得出c(Na+)= c(H2A)+2c(A2-),故D说法正确;
答案:C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
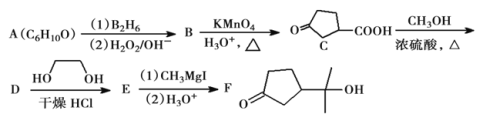
【题目】酯类化合物与格氏试剂(![]() ,
,![]() 、Br、I)的反应是合成叔醇类化合物的重要方法,可用于制备含氧多官能团化合物。化合物F的合成路线如下,回答下列问题:
、Br、I)的反应是合成叔醇类化合物的重要方法,可用于制备含氧多官能团化合物。化合物F的合成路线如下,回答下列问题:
已知:①![]()
②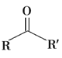
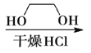
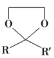
![]()
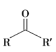
③![]()
![]()
![]()
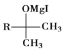
![]()
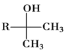
(1)A的结构简式为________;B中官能团的名称为________;![]() 的反应程式为________,其反应类型为________。
的反应程式为________,其反应类型为________。
(2)C与足量的![]() 反应后得到物质G,写出符合下列条件的G的同分异构体________(填结构简式,不考虑立体异构)。
反应后得到物质G,写出符合下列条件的G的同分异构体________(填结构简式,不考虑立体异构)。
①含有五元环结构;②能与![]() 溶液反应放出
溶液反应放出![]() 气体;
气体;
③![]() 与足量的钠反应,产生
与足量的钠反应,产生![]() 。
。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。用“*”标出化合物F中的手性碳原子。__________
(4)写出以![]() 、格氏试剂和
、格氏试剂和![]() 为原料制备的合成
为原料制备的合成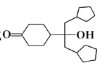 路线(其他试剂任选)。__________
路线(其他试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CH3COONa稀溶液中加入(或通入)少许X物质,其溶液中部分微粒浓度变化如下表所示(溶液温度不变):
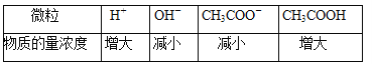
则X物质可能是( )
A.氯化氢B.氢氧化钠C.蒸馏水D.醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知难溶电解质在水溶液中存在溶解平衡MmAn(s)![]() mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料(25℃):
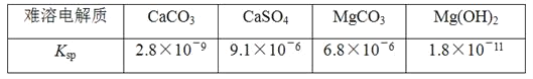
他们的实验步骤如下:
①往100mL0.1mol·L-1的CaCl2溶液中加入0.1mol·L-1的Na2SO4溶液100mL立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO33g,搅拌,静置后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越__(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式__。
(3)设计第③步的目的是什么__。
(4)请补充第④步操作及发生的现象__。
(5)请写出该转化在实际生活、生产中的一个应用__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol/L的NH4Br溶液中通人适量氨气呈中性,此时溶液中NH4+的数目为NA
B.25 °C时,Ksp (BaCO3)=2.5×10-9 ,则BaCO3饱和溶液中Ba2+ 的浓度为5×10-5 mol/L
C.100g 17%双氧水中含有H原子的数目为NA
D.28g N2和CO的混合气体中含有的氧原子的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,充分燃烧一定量的丁烷放出热量161.9kJ,经测定完全吸收生成的CO2需消耗5mol/L的KOH溶液100ml,恰好生成正盐,则此条件下热化学方程式:C4H10(g)+![]() O2(g)→4CO2(g)+5H2O(g)的△H为( )
O2(g)→4CO2(g)+5H2O(g)的△H为( )
A. +2590.4kJ/mol B. ﹣2590.4kJ/mol C. +1295.2kJ/mol D. ﹣1295.2kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH=4的硫酸溶液分别稀释成原体积的10倍、100倍、10000倍。则稀释后溶液的pH分别为( )
A.5、6、8B.5、6、7C.4.7、6.7、8D.4.7、6.7、7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂, 可由NO与Cl2在通常条件下反应得到。某学习小组在实验室用如图所示装置制备NOCl。
已知:亚硝酰氯(NOCl)的熔点为-64.5℃、沸点为-5.5℃, 气态呈黄色,液态时呈红褐色,易与水反应。
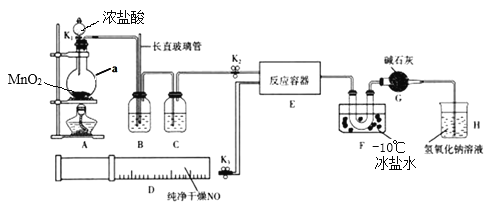
请回答下列问题:
(1)装置A中仪器a的名称是____________。
(2)实验开始时,应先打开K2,再打开____________(填K1”或K3”),通入一段时间气体,其目的是____________。
(3)实验时利用装置B除去某些杂质气体并通过观察B中的气泡来判断反应速率,装置B中的长直玻璃管还具有的作用是____________。
(4)装置C中应选用的试剂为____________(填试剂名称)。
(5)装置F的作用是____________。
(6)工业上可用间接电化学法除去NO,其原理如图所示,吸收塔中发生的反应为:NO+S2O42-+H 2O——N2+HSO3-(未配平)
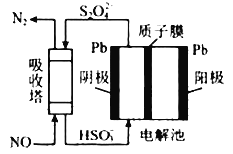
①吸收塔内发生反应的氧化剂与还原剂物质的量之比为________。
②阴极的电极反应式为_______。
(7)NOCl与H2O反应生成HNO2和HCl。请设计实验证明HNO2是弱酸:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com