
【题目】室温下,0.1 mol/L 的某二元酸 H2A 溶液中,可能存在的所有含 A 粒子的物质的量分数随 pH 变化的关系如图所示。下列说法不正确的是

A.H2A 的电离方程式:H2A=H+ + HA-
B.NaHA 溶液显酸性
C.等物质的量浓度的 NaHA 和Na2A 溶液等体积混合,离子浓度大小关系为:c(Na+)>c(A2-)>c(HA-)
D.pH = 5 时,在NaHA 和 Na2A 的混合溶液中: c(HA-) : c(A2-)= 100:1
【答案】D
【解析】
A.根据溶液中含有A2-和HA-离子,不存在H2A,则第一步电离完全;
B. 由A可知NaHA 溶液只发生电离不发生水解;
C.由图像可知pH=3时HA -和A2-浓度相等,则等物质的量浓度的 NaHA 和Na2A 溶液等体积混合pH<7,则电离大于水解;
D. 据图象分析,pH=3时,c(HA)与c(A2)相同,计算电离平衡常数K,再根据电离平衡常数计算pH = 5 时,计算c(HA-) : c(A2-)比值;
A. 根据溶液中含有A2-和HA-离子,不存在H2A,则第一步电离完全,H2A 的电离方程式:![]() ,故A正确;
,故A正确;
B. NaHA 溶液只发生电离不发生水解,则NaHA 溶液显酸性,故B正确;
C. .由图像可知pH=3时HA -和A2-浓度相等,则等物质的量浓度的 NaHA 和Na2A 溶液等体积混合pH<7,说明电离大于水解,所以c(Na+)>c(A2-)>c(HA-),故C正确;
D. 据图象分析,pH=3时,c(HA)与c(A2)相同.根据表达式:![]() ,pH=5时,结合K值可推出,c(HA):c(A2)=1:100,故D错误;
,pH=5时,结合K值可推出,c(HA):c(A2)=1:100,故D错误;
故答案选:D。


科目:高中化学 来源: 题型:
【题目】用惰性电极电解物质的量浓度相同、体积比为1∶3的 CuSO4和 NaCl的混合溶液,可能发生的反应有( )
①2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
③2Cl-+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
④2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
A. ①②③B. ①②④C. ②③④D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某硫酸试剂标签上的部分内容。下列说法错误的是( )

A.常温下,该硫酸可以用铁制容器运输
B.敞口放置的该硫酸因挥发而导致浓度变小
C.该硫酸的物质的量浓度为18.4molL﹣1
D.配制250mL0.4molL﹣1的稀硫酸需取该硫酸约5.4mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)密闭容器中mA(g)+nB(g)![]() pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
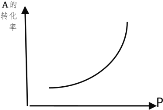
①增大压强,A的转化率___平衡向___移动,达到平衡后,混合物中C的浓度___。
②上述化学方程式中的系数m、n、p的正确关系是____。
③当降低温度时,C的浓度减小,正反应是___热反应。
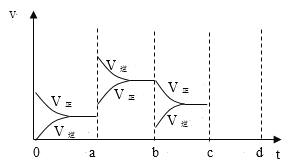
(2)如图表示在密闭容器中反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2S(g)+O2(g) = S2(s)+2H2O(l) △H= -632 kJmol-1,如图为质子膜H2S 燃料电池的示意图。下列说法正确的是

A.标准状况下,每 11.2 LH2S 参与反应,有1 mol H+经固体电解质膜进入正极区
B.电池工作时,电子从电极b 经过质子膜流向电极 a
C.电路中每流过 4 mol 电子,电池内部释放632 kJ 的热能
D.电极b 上发生的电极反应式为:O2+4e-+2H2O = 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电化学的叙述正确的是( )
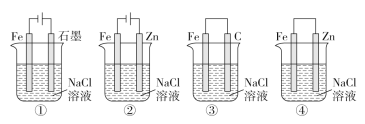
A. 图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B. 图②装置中Fe电极参与反应发生腐蚀
C. 图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D. 上述4个装置中,图①、②中Fe腐蚀速率较快,图③中Fe腐蚀速率较慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含钒石煤(含有铁、硅、铝、钙、镁等元素的氧化物)中的钒大部分是以V(III)和V(IV)形式存在,由含矾石煤提钒的一种工艺流程如图所示:

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
(1)含矾石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为__,最佳添加比例为__。

(2)如图为“抽滤”实验原理装置图,"抽滤”时抽气泵的作用是__;“酸浸渣”经“水洗涤”返回“浸出”的目的是__。

(3)已知酸浸液中V2O24+被H2O2氧化成VO2+,其离子方程式为__。“净化除杂”时用铜铁试剂除去所含的Al3+、Fe3+等杂质离子而不通过调节酸浸液pH的原因是__。
(4)“沉钒”的离子反应方程式为___。
(5)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%)。则A点对应物质的化学式为__,B点对应的物质为V2O5,则B点坐标为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.次氯酸钠中氯元素的化合价:+1
B.氟原子的结构示意图:![]()
C.明矾的化学式:KAlSO412H2O
D.硫酸的电离方程式:H2SO4=H2++SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)除去Na2CO3粉末中混入的NaHCO3杂质用__方法,化学方程式为__。
(2)除去氧化铜粉末中混入的氧化铝粉末通常用__试剂,离子方程式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com