
【题目】实验室常用下列图Ⅰ装置进行铜跟浓硫酸反应等一系列实验。
请回答:

(1)图I装置中的收集装置B应连接图Ⅱ中的__________(填“a”或“b”)进口。
(2)用此装置制SO2与将铜片直接加入试管A加热反应相比,其优点主要是______________。
(3)下列叙述中,描述正确的是______________。
A.A试管中发生了Cu与浓硫酸的反应,其中浓硫酸只体现了强氧化性
B.熄灭酒精灯后,因为A试管中的玻璃导管存在,整套装置不易发生倒吸
C.C试管中的紫色石蕊试液会变红,是因为二氧化硫溶于水后生成了 H2SO3
D.D、E试管中品红和高锰酸钾溶液都会褪色,其褪色原理相同
【答案】 b 方便控制反应的量及反应速率 BC
【解析】试题分析:(1)铜跟浓硫酸反应生成二氧化硫气体,二氧化硫密度大于空气,用向上排空气法收集;(2)通过抽插铜丝实现控制反应的量及反应速率;(3)A. Cu与浓硫酸的反应,生成硫酸铜、二氧化硫和水;熄灭酒精灯后, A试管中压强减小,空气由A试管中的玻璃导管进入A中;二氧化硫溶于水后生成了 H2SO3,能使石蕊变红;D试管中品红褪色是因为二氧化硫的漂白性;E试管中高锰酸钾溶液都会褪色,是因为二氧化硫的还原性。
解析:(1)铜跟浓硫酸反应生成二氧化硫气体,二氧化硫密度大于空气,用向上排空气法收集,B应连接图Ⅱ中的b进口;(2)通过抽插铜丝实现控制反应的量及反应速率;(3)A. Cu与浓硫酸的反应,生成硫酸铜、二氧化硫和水,浓硫酸表现酸性和氧化性,故A错误;熄灭酒精灯后, A试管中压强减小,空气由A试管中的玻璃导管进入A中,可以防倒吸,甘油B正确;二氧化硫溶于水后生成了 H2SO3,能使石蕊变红,故C正确;D试管中品红褪色是因为二氧化硫的漂白性;E试管中高锰酸钾溶液都会褪色,是因为二氧化硫的还原性,故D错误。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学设计了种用电解法制取Fe(OH)2的实验装置如图。通电后,溶液中产生白色沉淀,且较长时间不变色。下列说法中正确的是

A. 电源中"a"为正极," b"为负极
B. 电解池中的电解液可以是NaOH溶液但不能是NaCl溶液
C. A、B两端都必须使用铁作电极
D. B电极发生的反应:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
Zn(s)+1/2O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
Hg(l)+1/2O2(g)=HgO(s) ΔH2=-90.7 kJ·mol-1
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH3,其中ΔH3的值是
A. -441.8 kJ·mol-1 B. -254.6 kJ·mol-1
C. -438.9 kJ·mol-1 D. -260.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) +O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99KJ/mol。请回答下列问题:
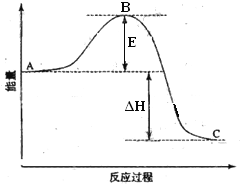
①图中A、C分别表示________、_______;
②E表示________;E的大小对该反应的反应热____(填“有”或“无”)影响。
③该反应通常用V2O5作催化剂,加V2O5会使图△H______(填“变大”、“变小”或“不变”),图中△H =______KJ/mol;
④已知单质硫的燃烧热为296 KJ/mol,计算由S(s)生成3molSO3(g)的△H=________KJ/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是
A. c(NH4+)>c(Cl–)>c(H+)>c(OH–) B. c(NH4+)>c(Cl–)>c(OH–)>c(H+)
C. c(Cl–)>c(NH4+)>c(H+)>c(OH–) D. c(Cl–)>c(NH4+)>c(OH–)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两串联电解池,左边放硫酸铜,右边放一定量的某硝酸盐溶液,电解时当左池有1.6g Cu析出时,右池析出0.45g固体,则右池溶质为:
A.AgNO3 B.NaNO3 C.Mg(NO3)2 D.Al(NO3)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,由下列实验事实得出结论错误的是
A.SO2使高锰酸钾溶液褪色,说明SO2具有漂白性
B.不小心将浓硫酸溅到手上,应立即用大量的水冲洗
C.常温下浓硫酸可以用铝罐储存,说明铝能在冷的浓硫酸中钝化
D.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是
A. Ca(OH)2的溶解度、溶剂的质量 B. 溶液中溶质的质量分数
C. 溶液的质量、水的电离平衡 D. 溶液中Ca2+的数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)某温度(t℃)时,水的Kw=10-13 mol2·L-2,则该温度(填大于、小于或等于) 25℃。将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,则:
(1)若所得混合液为中性,则a∶b ;
(2)若所得混合液的pH=2,则a∶b ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com