
| A. | 1:3 | B. | 3:1 | C. | 3:2 | D. | 1:2 |
分析 设转化的X为nmol,则
X(g)+3Y(g)?2Z(g)
开始 a b 0
转化 n 3n 2n
平衡 a-n b-3n 2n
平衡时,测得X和Y的转化率分别为25%和37.5%,
则$\frac{n}{a}$×100%=25%、$\frac{3n}{b}$×100%=37.5%,以此来解答.
解答 解:设转化的X为nmol,则
X(g)+3Y(g)?2Z(g)
开始 a b 0
转化 n 3n 2n
平衡 a-n b-3n 2n
平衡时,测得X和Y的转化率分别为25%和37.5%,
则$\frac{n}{a}$×100%=25%、$\frac{3n}{b}$×100%=37.5%,
解得a:b=1:2,
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握平衡三段法、转化率的计算为解答的关键,侧重分析与计算能力的考查,注意反应中物质转化量的关系,题目难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:解答题
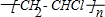 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
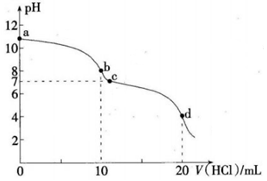
| A. | a、d 两点溶液中水电离出的c(H+):a<d | |
| B. | b点溶液存在:c(CO32-)+c(HCO3-)+c(H2CO3)=0.100mol/L | |
| C. | c点溶液存在:c(Na+)-c(Cl-)=c(HCO3-)+2c(CO32-) | |
| D. | b点溶液加水稀释过程中,溶液的pH不断升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | ||
| C. | H2(g)+O2(g)═H2O(l)△H=-285.8 kJ/mol | D. | H2(g)+O2(g)═H2O(g)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同质量的C和D单质分別与足量稀盐酸反应时,后者生成的氢气多 | |
| B. | C与D的最高价氧化物对应的水化物的碱性相比,后者更强 | |
| C. | 不用电解氯化物的方法制备单质D是由于其氯化物的熔点高 | |
| D. | 简单离子半径:B<C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y<Z<W | |
| B. | 原子最外层电子数:W>Z>Y | |
| C. | X、Y可以形成既有极性键也有非极性键的化合物 | |
| D. | 由X、Y、Z三种元素形成的化合物的水溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
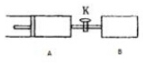 如图所示,向A、B中均充入1mol x、1mol Y,起始过A、B的体积都等于1L.在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0,达平衡时,A的体积为1.4L.下列说法错误的是( )
如图所示,向A、B中均充入1mol x、1mol Y,起始过A、B的体积都等于1L.在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0,达平衡时,A的体积为1.4L.下列说法错误的是( )| A. | 两容器中的反应分别达到平衡时,反应物X的速率:v(B)>v(A) | |
| B. | A容器中x的转化率为80% | |
| C. | 平衡时的压强:PA<PB | |
| D. | 平衡时Y体积分数:A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 LpH=l Ba(OH)2溶液中所含OH-的数目为0.2NA | |
| B. | 28g聚乙烯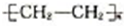 中含有的碳原子数为2NA 中含有的碳原子数为2NA | |
| C. | 1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的数目为NA | |
| D. | 1 mol Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子总数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com