
下表中有关离子方程式的评价合理的是
| 选项 | 化学反应及离子方程式 | 评价 |
| A | AlCl3溶液中加入过量氨水: Al3+ + 3NH3·H2O=Al(OH)3¯+3NH4+ | 错误,产物应该是 [Al(OH)4] - |
| B | 氯气与水反应: Cl2 + H2O == 2H+ + Cl- + ClO- | 正确 |
| C | 用氨水吸收过量二氧化硫: 2NH3·H2O + SO2=2NH4++SO32- + H2O | 正确 |
| D | 碳酸氢铵与足量NaOH溶液: NH4+ + OH- == NH3·H2O | 错误,漏掉了HCO3-与OH-的离子反应 |
科目:高中化学 来源: 题型:阅读理解
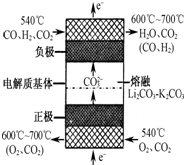 已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法: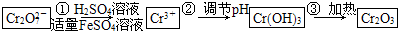
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
| O | 2- 7 |
| O | 2- 7 |
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下表中有关离子方程式的评价合理的是( )
选项 化学反应及离子方程式 评价
A AlCl3溶液中加入过量氨水:
Al3++3NH3·H2O=Al(OH)3¯+3NH4+ 错误,铝元素的产物应该是AlO2﹣
B 过量氯气通入溴化亚铁溶液中:
3Cl2+2Fe2++4Br- =6Cl- +2Fe3++2Br2 正确
C 用氨水吸收过量二氧化硫:
2NH3·H2O+SO2=2NH4++SO32-十H2O 正确
D 氯化铵溶于水:
NH4+ + 2H2O == H3O+ + NH3·H2O 错误,氯化铵溶解于水是物理变化,不能写离子方程式
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省五校协作体高三第二次联合模拟考试理综化学试卷(解析版) 题型:选择题
下表中有关离子方程式的评价合理的是 ( )
选项 化学反应及离子方程式 评价
A AlCl3溶液中加入过量氨水:
Al3++3NH3·H2O=Al(OH)3¯+3NH4+ 错误,铝元素的产物应该是AlO2﹣(或[Al(OH)4﹣])
B 过量氯气通入溴化亚铁溶液中:
3Cl2+2Fe2++4Br- =6Cl- +2Fe3++2Br2 正确
C 用氨水吸收过量二氧化硫:
2NH3·H2O+SO2=2NH4++SO32-十H2O 正确
D 氯化铵溶于水:
NH4+ + 2H2O = H3O+ + NH3·H2O 错误,氯化铵溶解于水是物理变化,不能写离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中有关离子方程式的评价合理的是( )
| 选项 | 化学反应及离子方程式 | 评价 |
| A | AlCl3溶液中加入过量氨水: Al3++3NH3·H2O=Al(OH)3¯+3NH4+ | 错误,铝元素的产物应该是AlO2﹣ |
| B | 过量氯气通入溴化亚铁溶液中: 3Cl2+2Fe2++4Br- =6Cl- +2Fe3++2Br2 | 正确 |
| C | 用氨水吸收过量二氧化硫: 2NH3·H2O+SO2=2NH4++SO32-十H2O | 正确 |
| D | 氯化铵溶于水: NH4+ + 2H2O == H3O+ + NH3·H2O | 错误,氯化铵溶解于水是物理变化,不能写离子方程式 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com