
【题目】下列实验误差分析正确的是
A. 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,读取滴定溶液体积偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度差偏小
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】以钛白副产品硫酸亚铁制备的铁黄(FeOOH)代替硝酸铁等可溶性铁盐制备高铁酸钾,可降低生产工艺成本且产品质量好。该制备工艺如下:
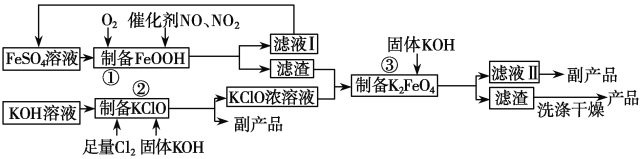
回答下列问题:
(1)写出该生产工艺中得到的副产品的一种用途:________________________。
(2)反应①的离子方程式为___________________________。
(3)反应③的化学方程式为2FeOOH+3KClO+4KOH===2K2FeO4+3H2O+3KCl,则流程中第一次加固体KOH的作用是______________________。第二次加固体KOH的作用是________________________。
(4)K2FeO4在水溶液中易“水解”:4FeO![]() +10H2O4Fe(OH)3+8OH-+3O2。则在洗涤干燥时,洗涤剂最好选用________(填序号)。
+10H2O4Fe(OH)3+8OH-+3O2。则在洗涤干燥时,洗涤剂最好选用________(填序号)。
a.H2O b.CH3COOK、异丙醇
c.NH4Cl、异丙醇 d.Fe(NO3)3、异丙醇
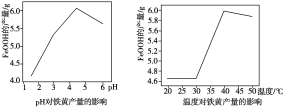
(5)实验测得反应液的pH、温度对铁黄产量的影响如图所示。为了获取更多的铁黄,反应液的pH应控制在________附近;反应液温度高于40 ℃时,铁黄的产量下降的原因可能是
________________________。
(6)用K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质。试写出K2FeO4处理含有NH3的污水时与NH3反应的离子方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某液态烃的分子式为CmHn,相对分子质量为H2的39倍。它不能使酸性高锰酸钾溶液褪色,不能使溴的四氯化碳溶液因反应而褪色。在催化剂存在时,7.8 g该烃能与0.3 mol H2发生加成反应生成相应的饱和烃CmHp。则
(1)m、n、p的值分别是m=________,n=________,p=________。
(2)CmHp的结构简式是__________________。
(3)CmHn能和浓硫酸、浓硝酸的混合酸反应,该反应的化学方程式是___________________,
该反应属于________反应,有机产物的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知质子数或中子数为奇数的原子核才有NMR现象,而质子数和中子数均为偶数的原子不产生核核磁共振,下列原子组一定能产生NMR现象的是( )
A. 18O、31P、119Sn B. 27Al、19F、12C
C. 6C、16S、9F D. 1H、13C、35Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 分子晶体中一定存在分子间作用力,不一定存在共价键
B. 分子中含两个氢原子的酸一定是二元酸
C. 含有共价键的晶体一定是分子晶体
D. 元素的非金属性越强,其单质的活泼性一定越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.某元素从化合态变成游离态,该元素一定被还原
C.由同种分子构成的物质一定是纯净物
D.电离时能生成H+的化合物一定是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
pH=8![]()
![]()
![]()
![]()
(1)实验①可说明________(填字母)。
a.该Na2S2O3溶液中水电离的c(OH-)=10-8mol·L-1
b.H2S2O3是一种弱酸
c.Na2S2O3是一种弱电解质
d.Na2S2O3的水解方程式为S2O![]() +2H2OH2S2O3+2OH-
+2H2OH2S2O3+2OH-
(2)写出实验②发生反应的离子方程式:_____________________________。
(3)Na2S2O3溶液中加入盐酸有淡黄色沉淀和刺激性气味的气体生成,写出该反应的离子方程式:_________________________________。
(4)实验室制得的Na2S2O3·5H2O粗产品中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O的含量,一般在酸性条件下用KMnO4标准溶液滴定(假设粗产品中杂质与酸性KMnO4溶液不反应)。称取1.28 g粗样品溶于水,用0.40 mol·L-1 KMnO4标准溶液(加入适量硫酸酸化)滴定,当溶液中S2O![]() 全部被氧化时,消耗KMnO4溶液体积20.00 mL(5S2O
全部被氧化时,消耗KMnO4溶液体积20.00 mL(5S2O![]() +8MnO
+8MnO![]() +14H+===8Mn2++10SO
+14H+===8Mn2++10SO![]() +7H2O)。试回答:
+7H2O)。试回答:
①此滴定实验是否需要指示剂?_______(填“是”或“否”)。KMnO4溶液置于________(填“酸式”或“碱式”)滴定管中。
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果________(填“偏高”“偏低”或“不变”)。
③产品中Na2S2O3·5H2O的质量分数为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com