
【题目】某核素 ![]() 可形成HmX型氢化物,则 a g HmX 含有( )
可形成HmX型氢化物,则 a g HmX 含有( )
A.![]() mol质子
mol质子
B.![]() mol电子
mol电子
C.![]() mol中子
mol中子
D.![]() mmol HmX
mmol HmX
【答案】A
【解析】解:核素 ![]() 的质子数为Z,质量数为A,故中子数为(A﹣Z).故HmX的摩尔质量为(A+m)g/mol,故agHmX的物质的量n=
的质子数为Z,质量数为A,故中子数为(A﹣Z).故HmX的摩尔质量为(A+m)g/mol,故agHmX的物质的量n= ![]() mol. A.由于HmX中含(Z+m)个质子,故
mol. A.由于HmX中含(Z+m)个质子,故 ![]() molHmX中含
molHmX中含 ![]() (Z+m)mol质子,故A正确;
(Z+m)mol质子,故A正确;
B.分子中质子数等于电子数,所以含 ![]() (Z+m)mol电子,故B错误;
(Z+m)mol电子,故B错误;
C.由于H原子不含中子,故HmX中含(A﹣Z)个中子,所以含 ![]() (A﹣Z)mol中子,故C错误;
(A﹣Z)mol中子,故C错误;
D.HmX的摩尔质量为(A+m)g/mol,agHmX的物质的量n= ![]() mol,故D错误;
mol,故D错误;
故选A.
核素 ![]() 的质子数为Z,质量数为A,故中子数为(A﹣Z).故HmX的摩尔质量为(A+m)g/mol,据此求出agHmX的物质的量,然后结合HmX中含(Z+m)个质子、电子,(A﹣Z)个中子来分析.
的质子数为Z,质量数为A,故中子数为(A﹣Z).故HmX的摩尔质量为(A+m)g/mol,据此求出agHmX的物质的量,然后结合HmX中含(Z+m)个质子、电子,(A﹣Z)个中子来分析.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有200mLMgCl2和AlCl3的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl﹣)为1.3mol/L,要使Mg2+与Al3+完全分离,至少需加4mol/L的NaOH溶液的体积为( )
A.40mL
B.72mL
C.80mL
D.128mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥分析下列氧化还原反应中化合价变化、得失电子情况,并指出氧化剂和还原剂是什么.
(1)H2+CuO═Cu+H2O;上面反应中,氧化剂是:还原剂是: , “双线桥”表示电子转移方向及数目为
(2)C+2CuO═2Cu+CO2↑;该反应中氧化剂是:还原剂是: . 双线桥法为: ,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,A,B中的电极为多孔的惰性电极;C,D为夹在湿的Na2SO4滤纸条中心的铂夹;电源有a、b两极.若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1 , 闭合K2、K3通直流电,则:①标出电源的正、负极,a为极,b为极.
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象 .
③写出电极反应式:
A中 .
B中 .
④若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3 , 闭合K1 , 则电流表的指针是否移动(填是或否) . 若电流表指针不移动说明理由,若指针移动也说明理由 . 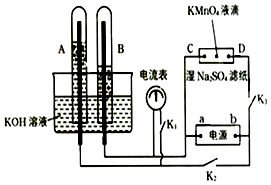
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示与对应叙述相符的是( )

A. 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X + 3Y![]() Z
Z
B. 图2表示NaOH溶液滴加到0.1 mol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂
C. 常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图3所示。当7<pH<13 时,溶液中c(Na+)>c(CH3COO->c(OH-)>c(H+)
D. 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图4可确定首先沉淀的是C-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解.实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.实验室制取时,将工业用氢氧化钙(含铜离子等杂质)和甲醛依次加入到质量分数为30﹣70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是 .
(2)反应温度最好控制在30﹣70℃之间,温度不易过高,其主要原因是 .
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是 .
(4)实验时需强力搅拌45min,其目的是;结束后需调节溶液的pH 7~8,其目的是 . 最后经结晶分离、干燥得产品.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中正确的是( )
A.铁与盐酸的反应:2Fe+6H+=2Fe3++3H2↑
B.石灰石与稀盐酸反应制备二氧化碳:CO ![]() +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
C.向氢氧化铜中滴加硫酸溶液:H++OH﹣=H2O
D.硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO ![]() +Ba2++2OH﹣=Cu(OH)2↓+BaSO4↓
+Ba2++2OH﹣=Cu(OH)2↓+BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com