
3��5-����������������Ҫ���л��ϳ��м��壬��������Ȼ���ʰ������صĺϳɡ�һ���Լ䱽����Ϊԭ�ϵĺϳɷ�Ӧ���£�

�״������Ѻ�3��5-�����������ӵIJ����������ʼ��±���
| ���� | �е�/�� | �۵�/�� | �ܶ�(20��) / g·cm-3 | �ܽ��� |
| �״� | 64. 7 |
| 0. 7915 | ������ˮ |
| ���� | 34. 5 |
| 0. 7138 | ����ˮ |
| 3��5-������������ |
| 33 ~36 |
| �����ڼ״������ѣ�����ˮ |
��1����Ӧ�������ȷ�����״����ټ������ѽ�����ȡ���ٷ�����״��IJ����ǵ� ��
����ȡ�õ��ķ�Һ©��ʹ��ǰ�� ��ϴ������Һʱ�л����ڷ�Һ©���� ����ϡ����¡����㡣
��2������õ����л��������ñ���NaHCO3��Һ������ʳ��ˮ����������ˮ����ϴ�ӡ��ñ���NaHCO3 ��Һϴ�ӵ�Ŀ���� ���ñ���ʳ��ˮϴ�ӵ�Ŀ���� ��
��3��ϴ����ɺ�ͨ�����²������롢�ᴿ�����ȷ�IJ���˳���� (����ĸ)��
a�������ȥ���� b�����ؽᾧ c�����˳�ȥ����� d��������ˮCaCl2����
��4����Һ���볣���ü�ѹ���ˡ�Ϊ�˷�ֹ��������ѹ������ɺ�Ӧ�� ���� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л����������ӳɷ�Ӧʹ��ˮ��ɫ������ʹKMnO4������Һ��ɫ����(����)
A�����顡���������������� B���Ҵ�
C����ϩ(CH3CH===CH2) D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʼ��������Լ�����ȷ����(����)
A���Ҵ���������CaCO3����
B���������ϩ��NaOH��Һ
C������CCl4�ͼ�����ˮ
D����ϩ����������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ӳ�ʲ������ǻ�ѧʵ���о���ʹ�õ�һ�����������������ʵ�飨�̶�װ���ԣ����ش����⡣
������ʵ�飺��ͼ��ʾ����Ũ�������װ��Na2SO3�����������һ��ʱ���a��b��c��������仯���±�������д���еĿհף�
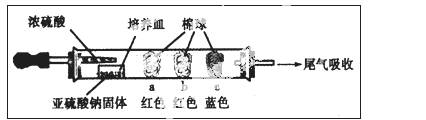
| ���� | �����ϵμӵ��Լ� | ʵ������ | ���ͺͽ��� |
| a |
| �����ף��Ⱥ��ָֻ���ɫ |
|
| b | ����̪��NaOH��Һ | �����Ϊ��ɫ | ���ӷ���ʽ�� |
| c |
| �����Ϊ��ɫ | ��������� (ѡ������ԡ���ԭ�ԡ�) |
��Ӳ�ʲ�����������װ�ý����ɶ��Ի���ʵ�顣��ͼ��ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����װ�á�
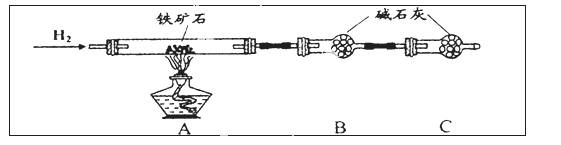
ʵ��һ������ʯ�к������IJⶨ
��1������ͼ��װ����(�г�������ʡ��)�����װ�õ������ԣ�
��2����10��0g����ʯ����Ӳ�ʲ������У�
��3������˵����ܿڴ����ϵػ���ͨ��H2�� ��ȼA���ƾ��ƣ�
��4����ַ�Ӧ�����ƾ��ƣ��ٳ���ͨ����������ȫ��ȴ��
��5����÷�Ӧ��װ��B����2.70g��������ʯ��������������Ϊ______________________��
ʵ���������ʯ�к������IJⶨ
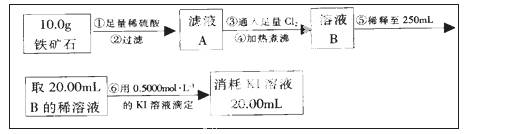
��1������ں͢��ж�Ҫ�õ��IJ��������� __��
��2�������йز���IJ�����˵������ȷ����_______��
a���ζ���������ˮϴ�Ӻ����ô�װҺ��ϴ
b����ƿ��Ҫ�ô���Һ��ϴ
c����Ϊ��ˮΪ��ɫ�����Եζ������в����ָʾ��
ʵ����ۣ������������������ɣ���ʵ��һ�����ó�������ʯ������������Ļ�ѧʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������һ����Ҫ�Ļ�����Ʒ��ij��ȤС�����Ʊ���������ƾ��壨Na2S2O3·5H2O����
I��[��������]
��1��Na2S2O3·5H2O����ɫ�����壬������ˮ����ϡ��Һ��BaCl2��Һ����������ɡ�
��2����Na2CO3��Na2S���Һ��ͨ��SO2���Ƶ�Na2S2O3�����ò�Ʒ�г���������Na2SO3��Na2SO4��
��3��Na2SO3�ױ�������BaSO3������ˮ��������ϡHCl��
��[�Ʊ���Ʒ]
ʵ��װ����ͼ��ʾ��ʡ�Լг�װ�ã�
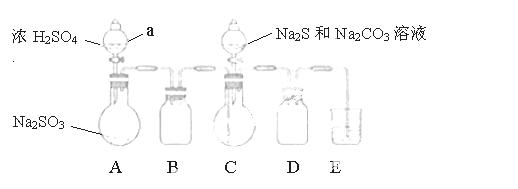
ʵ�鲽�裺
��1�����װ�������ԣ���ͼʾ�����Լ�������a��������____��E�е��Լ���___��ѡ��������ĸ��ţ���
A��ϡH2SO4 B��NaOH��Һ C������NaHSO3��Һ
��2������C����ƿ����Na2S��Na2CO3�����Һ������A����ƿ�μ�ŨH2SO4��
��3����Na2S��Na2CO3��ȫ���ĺ�����Ӧ������C�л��Һ����Һ��____����д�������ƣ����ᾧ�����ˡ�ϴ�ӡ�����õ���Ʒ��
��[̽���뷴˼]
��1��Ϊ��֤��Ʒ�к���Na2SO3��Na2SO4����С�����������ʵ�鷽�����뽫���������������������Լ���ϡHNO3��ϡH2SO4��ϡHCl������ˮ��ѡ��
ȡ������Ʒ���ϡ��Һ���μ�����BaCl2��Һ���а�ɫ�������ɣ�_____��������δ��ȫ�ܽ⣬���д̼�����ζ��������������ȷ����Ʒ�к���Na2SO3��Na2SO4��
��2��Ϊ����װ��C�����ɵ�Na2SO4�������ڲ��ı�ԭ��װ�õĻ����϶�ԭ��ʵ�鲽�裨2�������˸Ľ����Ľ���IJ�����_______��
��3��Na2S2O3·5H2O���ܽ�����¶����������������ò�Ʒͨ��_____�����ᴿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������������������ɵĻ�����У�����2mol/L������Һ65mL��ǡ����ȫ��Ӧ��������Һ��Fe2+�ܱ���״����112mL������������ԭ������н���Ԫ�غ���Ԫ�ص�ԭ�Ӹ���֮��Ϊ��������
| �� | A�� | 5��7 | B�� | 4��3 | C�� | 3��4 | D�� | 9��13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ�ǣ�������
| �� | A�� | ��̼������Һ����������������2CO32��+SO2+H2O=2HCO3��+SO32�� |
| �� | B�� | ����������������Al+2H+=Al3++H2�� |
| �� | C�� | ��������ˮ�У�S2��+2H2O=H2S��+2OH�� |
| �� | D�� | ̼��þ���������У�CO32��+2H+=H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�в�����ȡ����Ӧ����(����)
A���ڴ������ڵ������£������巴Ӧ���屽
B������Ũ���ᡢŨ�����Ϲ�����������
C����������������Ϻ����
D����һ�������£���ϩͨ��һ���ķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������ȷ���ǣ� ��
A����¯�г�����CaSO4����Na2CO3��Һ���ݺ��ٽ������������ܽ�ȥ��
B�����ˮ�еμ�FeCl3������Һ�Ʊ�Fe(OH)3�����ԭ���Ǽ��ȴٽ���Fe3+ˮ��
C����ˮ�м���������¶���ʹˮ�����ӻ���С������ƽ�������ƶ�
D����Ӧ2A(g) + B(g)��3C (s) + D(g)��һ�����������Է����У�˵���÷�Ӧ�Ħ�H>0
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com