
����Ŀ����֪������,Ka1(H2CO3)=4.3��10-7,Ka2(H2CO3)=5.6��10-11��ij��Ԫ��H2R�������ε���Һ��,H2R��HR-��R2-���ߵ����ʵ�����������ҺpH�仯��ϵ��ͼ��ʾ����������������ǣ� ��

A. ��pH=4.3����Һ�У�3c(R2-)=c(Na+)+c(H+)-c(OH-)
B. ���������Ũ�ȵ�NaOH��Һ��H2R��Һ��Ϻ���Һ��ˮ�ĵ���̶ȱȴ�ˮС
C. ��Ũ�ȵ�NaOH��Һ��H2R��Һ�������1��2���,��Һ��pH=1.3
D. ��Na2CO3��Һ�м�������H2R��Һ��������Ӧ��2CO32-+H2R=2HCO3-+R2-
���𰸡�C
��������A.��pH=4.3����Һ�У�c(R2)=c(HR)��2c(R2)+c(HR)+c(OH)=c(Na+)+c(H+)������3c(R2-)=c(Na+)+c(H+)-c(OH-)����A��ȷ��B. �������Ũ�ȵ�NaOH��Һ��H2R��Һ��Ϻ����ɵ�Ũ�ȵ�H2R��HR����Һ��pH=1.3����Һ�����ԣ���ˮ�ĵ������������ã�������Һ��ˮ�ĵ���̶ȱȴ�ˮС����B��ȷ��C.��ͼ��֪����Ũ�ȵ�NaOH��Һ��H2R��Һ�������1��1��Ϻ�,��Һ��pH=1.3����C����D.��pH=1.3ʱ��c(HR)=c(H2R)����H2R��K1=![]() =101.3mol/L����pH=4.4ʱ��c(HR)=c(R2)����H2R��K2=
=101.3mol/L����pH=4.4ʱ��c(HR)=c(R2)����H2R��K2=![]() =104.4mol/L����H2CO3��Ka1=4.2��107,Ka2=5.6��1011���ʿ�֪����ǿ����ϵ��H2R>HR>H2CO3>HCO3������Na2CO3��Һ�м�������H2R��Һ������R2�������ӷ���ʽΪ2CO32-+H2R=2HCO3-+R2-����D��ȷ����ѡC.
=104.4mol/L����H2CO3��Ka1=4.2��107,Ka2=5.6��1011���ʿ�֪����ǿ����ϵ��H2R>HR>H2CO3>HCO3������Na2CO3��Һ�м�������H2R��Һ������R2�������ӷ���ʽΪ2CO32-+H2R=2HCO3-+R2-����D��ȷ����ѡC.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20mL��ijϡH2SO4��Һ�е���0.1mol/L��ˮ����Һ��ˮ�����������Ũ������백ˮ����仯��ͼ�����з�����ȷ����
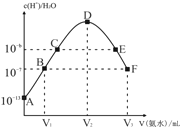
A. ϡ�����Ũ��Ϊ0.1mol/L
B. C���E����Һ��pH=14-a
C. c��NH4+��/c(NH3��H2O)��B��>F��
D. E��Һ�д���c��NH4+��>c��SO42-��> c��OH-��> c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ɢϵ��ʵ������ǣ�������
A.��۳�����
B.��������
C.���ȶ�
D.��ɢ������ֱ���Ĵ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ǿ�ᣬ��ѧ�ν�������ˮ��Һ�п�����ȫ���롣����ʵ�ǣ�������ˮ�еĵ�һ����������ȫ�ģ��ڶ������벢����ȫ����������ΪH2SO4==H++HSO4-��HSO4-![]() H++SO42-����ش������й�����:
H++SO42-����ش������й�����:
(1)Na2SO4��Һ��_______(������ԡ������ԡ��������ԡ�)����������(�����ӷ���ʽ��ʾ)_____________��
(2)H2SO4��Һ��BaCl2��Һ��Ӧ�����ӷ���ʽΪ____________________________________��
(3)��:0.10mol/L��Na2SO4��Һ�У���������Ũ�ȹ�ϵȷ����____(����ĸ)
A.c(Na+)=c(SO42-)+c(HSO4-)+c(H2SO4)
B.c(OH-)=c(HSO4-)+c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-)
D.c(Na+)=2c(SO42-)+2c(HSO4-)
(4)��25��ʱ��0.10mol/L��NaHSO4��Һ��c(SO42-)=0.029mol/L����0.10mol/L��H2SO4��Һ��c(SO42-)___(�<����>����=��)0.029mol/L
(5)��25��ʱ��0.10mol/LH2SO4��Һ��pH=-lg0.11,��0.10mol/LH2SO4��Һ��c(SO42-)=____mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������Ӽ��ɵ�·�Ļ������ϡ��û�ѧ�������Ƶøߴ��ȹ裬�仯ѧ����ʽΪ��
��SiO2��2C![]() Si��2CO������Si��2Cl2
Si��2CO������Si��2Cl2![]() SiCl4
SiCl4
��SiCl4��2H2![]() Si��4HCl��
Si��4HCl��
���ж�����������Ӧ�������У�����ȷ����
A. �٢�Ϊ�û���Ӧ
B. ��Ϊ���Ϸ�Ӧ
C. �٢ڢ۾�Ϊ������ԭ��Ӧ
D. ������Ӧ�ķ�Ӧ���й�Ԫ�ؾ�����ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(POCl3)�������뵼����Ӽ������άԭ��,ʵ�����Ʊ�POCl3���ⶨ��Ʒ������ʵ��������£�
���Ʊ�POCl3��
������������Һ̬PCl3����ȡPOCl3,ʵ��װ��(���ȼ��г�������)��ͼ��ʾ��
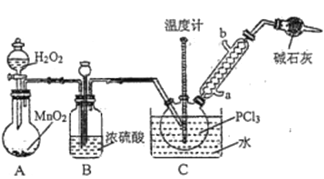
��֪����Ag++SCN-=AgSCN��;Ksp(AgCl)>Ksp(AgSCN);�������������ᡣ
��PCl3��POCl3�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | -112.0 | 76.0 | 137.5 | ������,��Ϊ��ɫҺ��,��ˮ�����ҷ�Ӧ���ɺ�������Ȼ��� |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)POCl3��ˮ��Ӧ�Ļ�ѧ����ʽΪ_________________________________________��
(2)װ��B�����ó�����O2��,����_________________________________________������ܵ�������_______________��
(3)��Ӧ�¶�Ҫ������60~65��,ԭ����_____________________________________________��
�ⶨPOCl3��Ʒ�ĺ�����
ʵ�鲽�裺
���Ʊ�POCl3ʵ�������������ƿ�е�Һ����ȴ�����£�ȷ��ȡ30.7gPOCl3��Ʒ,����ʢ��60.00mL����ˮ��ˮ��ƿ��ҡ������ȫˮ��,��ˮ��Һ���100.00mL��Һ��
��ȡ10.00mL��Һ����ƿ��,����10.00mL3.2mol/LAgNO3����Һ��
�ۼ�����������������ҡ����ʹ�������汻�л��︲�ǡ�
����XΪָʾ��,��0.2mol/LKSCN��Һ�춨������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥ10.00mLKSCN��Һ��
(4)������м�����������������___________________________________________�����˲���,�����Ʒ����Ԫ�ص�������������__________(�ƫ����ƫС�����䡱)��
(5)�������XΪ__________,��Ʒ��POCl3����������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Ti)����Ϊ��������֮��ĵ����������Ѱ�(TiO2)��Ŀǰ��õİ�ɫ���ϡ��Ʊ�TiO2��Ti��ԭ�����������ҹ�������������������λ���ú���Fe2O3��������(��Ҫ�ɷ�ΪFeTiO3)��ȡTiO2���������£�
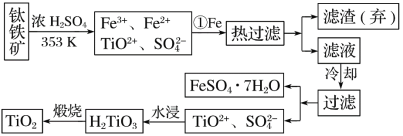
��1������ټ�Fe��Ŀ����________________________________________________________���������ȴ��Ŀ����________________________________________________________��
��2�������Ʊ�TiO2�Ĺ����У��������õĸ�������______________________��
��3���ɽ��ʯ(TiO2)��ȡ����Ti���漰���IJ���ΪTiO2�D��TiCl4![]() Ti����ӦTiCl4��2Mg===2MgCl2��Ti��Ar�����н��е�������_________________________��
Ti����ӦTiCl4��2Mg===2MgCl2��Ti��Ar�����н��е�������_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з�Ӧ�У����������뻹ԭ����Ϊͬһ���ʵ���
A. Cl2��2NaOH===NaCl��NaClO��H2O
B. MnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2��
MnCl2��2H2O��Cl2��
C. Fe��2HCl===FeCl2��H2��
D. KClO3��6HCl(Ũ)===KCl��3Cl2����3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ����
A. ij���ӱ�������ȫ��ָ����������Һ�е�Ũ�ȱ�Ϊ0
B. ij���ʵ��ܽ���Ϊ���ܣ�������ʵ��ܽ��Ϊ0
C. һ����˵���ܽ��С������������ת��Ϊ�ܽ�ȴ��������
D. ���������ɡ��ܽ��ת����ʵ�ʶ��dz����������ܽ�ƽ����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com