
下列叙述正确的是( )
A.同一周期元素的原子,半径越小越容易失去电子
B.元素的性质呈周期性变化的根本原因是核外电子排布呈周期性变化
C.第IA族元素与第VIIA族元素形成的化合物都是离子化合物
D.元素周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年湖北省宜昌市高一下期中化学试卷(解析版) 题型:推断题
有A、B、C、D 4种短周期元素,它们的元素原子序数依次增大,由B、C、D形成的离子具有相同的电子层结构。B原子的最外层电子数是次外层的三倍,C、D单质都能跟水剧烈反应,1 mol D单质跟水反应产生11.2 L(标准状况)A气体,此时D转化为具有氖原子核外电子层结构的离子。试填写:
(1)用电子式表示A和C形成化合物的过程______________。
(2)C原子的结构示意图_______________,写出A、B两元素按1:1原子个数比形成化合物的电子式_______________。
(3)这4种元素的原子半径由大到小的顺序为_______________。(用元素符号表示)
(4)写出C单质与水反应的化学反应方程式__________________________;。
(5)写出D单质与水反应的离子方程式__________________________,
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:填空题
有A、B、C、D、E五种短周期元素, 它们的原子序数依次增大。 已知A和B原子具有相同的电子层数, 且A的最外层电子数是次外层电子数的两倍, C是该周期中原子半径最大的元素, C的单质在加热下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻。 试根据以上叙述回答:
 (1)元素名称: A C __________ E
(1)元素名称: A C __________ E

 (2)写出AB2与过量氢氧化钠溶液反应的离子方程式 ;
(2)写出AB2与过量氢氧化钠溶液反应的离子方程式 ; 写出 C2B2与AB2反应的化学方程式
写出 C2B2与AB2反应的化学方程式
 ;
;

 (3)画出D的原子结构示意图 ,
(3)画出D的原子结构示意图 ,
 用电子式表示化合物 C2D 的形成过程 ;
用电子式表示化合物 C2D 的形成过程 ;
 (4)D、E的气态氢化物的稳定性 大于 (填化学式)。
(4)D、E的气态氢化物的稳定性 大于 (填化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
在一定条件下的密闭容器中发生反应:C(s)+CO2(g)=2CO(g)。下列说法不正确的是( )
A.将碳块磨成粉末可加快反应速率
B.增加碳的质量可加快反应速率
C.升高温度可加快反应速率
D.容器体积不变时,向容器中充入氦气,反应速率不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
下列化学用语表述正确的是( )
A.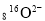 的结构示意图:
的结构示意图: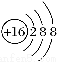
B.NH4Br的电子式:
C.CCl4的结构式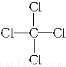
D.氧元素基态原子的电子排布式:1s22s12p3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
某同学为验证元素周期表中元素性质的递变规律,利用右图装置可验证同主族非金属性的变化规律。设计了如下系列实验。
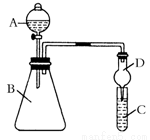
(1)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____________________________________________。
(2)仪器A的名称为____________________,
(3)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4, (KMnO4 与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到混合溶液 的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______________ 溶液吸收尾气。
(4)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3,C中加Na2SiO3 溶液观察到C中溶液_____________的现象,即可证明。但有的同学认为盐酸具有挥发性,应用__________溶液除去。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
A.不用稀硫酸,改用98%浓硫酸 B.加热
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省徐州市高二下第二次质量检测化学试卷(解析版) 题型:填空题
为比较温室效应气体对全球增温现象的影响,科学家以CO2为相对标准,引入了“温室效应指数”的概念(如下表)。
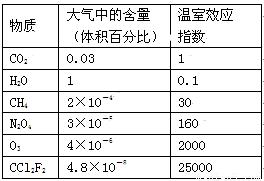
回答下列问题:
(1)6种气体中,温室效应指数最大的物质属于 (选填“极性分子”或“非极性分子”)。
(2)1mol CO2中σ键的数目为 ,由第二周期原子构成与CO2互为等电子体的分子是 ,阴离子是 。(写一种)
(3)水的沸点高于CO2的原因是 ,冰熔化时体积变小密度变大的原因是 。
(4)配合物Fe (CO)5结构式如图:
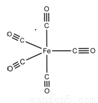
配合物中碳原子的轨道杂化类型是 ;1mol Fe (CO)5分子中含有σ键的数目为 ,将配位键的共价键上加上箭头。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高一下学期第二次月考化学试卷(解析版) 题型:填空题
按下列要求书写反应方程式,有要求的要注明反应类型。
1、乙烯与Br2的反应: 。反应类型: 。
2、乙烯制聚乙烯 :
3、苯与液溴的反应 : 。反应类型: 。
4、乙醇与金属钠的反应:
5、乙醇的催化氧化反应:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com