
| A. | 乙烯能使酸性高锰酸钾溶液褪色,甲烷则不能使其褪色 | |
| B. | 溶于水能导电的化合物不一定是离子化合物 | |
| C. | 需要加热的反应不一定是吸热反应 | |
| D. | 石油的分馏和煤的干馏都是化学变化 |
分析 A、碳碳双键能被高锰酸钾氧化;
B、化合物溶于水能导电只能说明其溶于水后能电离出自由移动的离子;
C、需要加热的反应不一定是吸热的;
D、煤的干馏是将煤隔绝空气加强热使煤分解的过程.
解答 解:A、碳碳双键能被高锰酸钾氧化,故乙烯能将高锰酸钾溶液还原,从而高锰酸钾溶液褪色,而甲烷不能被高锰酸钾溶液氧化,故不能使高锰酸钾溶液褪色,故A正确;
B、化合物溶于水能导电只能说明其溶于水后能电离出自由移动的离子,与其是离子化合物还是共价化合物无关,故HCl溶于水后能导电,但其是共价化合物,故B正确;
C、需要加热的反应不一定是吸热的,如煤炭的燃烧,需要加热才能发生,但是放热反应,故C正确;
D、煤的干馏是将煤隔绝空气加强热使煤分解的过程,故煤的干馏是复杂的化学变化过程,故D错误.
故选D.
点评 本题考查了烯烃和烷烃的性质、反应条件与吸放热反应间的关系以及煤和石油的综合利用等,应注意的是不能根据反应条件来判断反应吸放热.


科目:高中化学 来源: 题型:选择题
| A. | 1:2:l | B. | 2:2:1 | C. | 2:3:l | D. | 4:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有Al3+、Mg2+、NO3-,可能有NH4+、K+ | |
| B. | 肯定有Al3+、K+、Cl-,肯定没有MnO4-、Mg2+ | |
| C. | 肯定有Al3+、NH4+、Cl-、NO3-,一定没有HCO3-、Mg2+、MnO4- | |
| D. | 该溶液可能显弱酸性,也可能显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
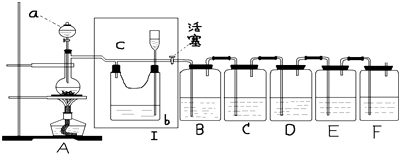
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol A、2mol B | 6mol A、4mol B | 2mol C |
| 到达平衡的时间(min) | 5 | 8 | |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | w3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
| A. | 若x<4,则2c1>c2 | |
| B. | 若x=4,则w3=w1 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
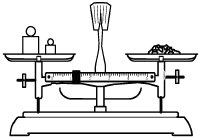 | 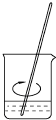 | 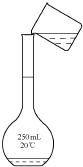 |  |
| A.称量 | B.溶解 | C.转移 | D.摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体带电荷,而溶液呈电中性 | |
| B. | 胶体加入电解质可产生沉淀,而溶液不能 | |
| C. | 胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 | |
| D. | 胶体能够发生丁达尔现象是因为光的反射 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com