
 .
. .
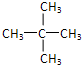
.分析 (1)先利用减链法书写同分异构体,然后根据不能由某种烯烃和氢气加成获得判断碳原子上氢原子的种类写出结构简式;
(2)属于芳香烃,则含有1个苯环,剩余3个C,可以是丙基、甲基和乙基或者3个甲基,一溴代物只有2种,说明有2类氢原子,苯环上只有一种H;
(3)C4H10的同分异构体有:CH3CH2CH2CH3、CH3CH(CH3)CH3,利用1个Cl原子替换H原子,分析在NaOH乙醇溶液中加热发生消去反应其符合条件的结构;
(4)1,2-二溴乙烷在氢氧化钠醇溶液、加热条件下发生消去反应生成乙炔;
解答 解:(1)戊烷的同分异构体:所有的碳原子在一条链上:CH3-CH2-CH2-CH2-CH3;拿下1个碳原子作为支链: ;拿下2个碳原子作为支链:
;拿下2个碳原子作为支链: ;其中不能由某种烯烃和氢气加成获得,说明有碳上无氢原子即只有一种氢原子,为
;其中不能由某种烯烃和氢气加成获得,说明有碳上无氢原子即只有一种氢原子,为 ,
,
故答案为: ;
;
(2)B是苯的同系物,分子式为C9H12,含有1个苯环,剩余3个C,可以是丙基、甲基和乙基或者3个甲基,一溴代物只有2种,说明有2类氢原子,苯环上只有一种H,则为间三甲苯,其结构简式为 ,
,
故答案为: ;
;
(3)C4H10的同分异构体有:CH3CH2CH2CH3、CH3CH(CH3)CH3,CH3CH2CH2CH3的一氯取代产物有两种:CH3CH2CH2CH2Cl、CH3CH(Cl)CH2CH3,CH3CH(CH3)CH3的一氯取代产物也有两种: 和(CH3)2CHCH2Cl,CH3CH2CH2CH2Cl、
和(CH3)2CHCH2Cl,CH3CH2CH2CH2Cl、 和(CH3)2CHCH2Cl的消去产物都只有一种,所以只有CH3CH(Cl)CH2CH3符合;
和(CH3)2CHCH2Cl的消去产物都只有一种,所以只有CH3CH(Cl)CH2CH3符合;
故答案为:CH3CH(Cl)CH2CH3;
(4)CH2BrCH2Br在氢氧化钠醇溶液、加热条件下发生消去反应:CH2BrCH2Br+2NaOH$→_{△}^{醇}$CH≡CH↑+2NaBr+2H2O,
故答案为:CH2BrCH2Br+2NaOH$→_{△}^{醇}$CH≡CH↑+2NaBr+2H2O.
点评 本题考查有机物结构简式的确定、烯的性质等,题目难度中等,注意同分异构体个数的判断、注意苯环上取代基位置的确定是解决本题的关键.


科目:高中化学 来源: 题型:多选题
| A. | 加H2O | B. | 滴入几滴浓盐酸 | ||
| C. | 增大压强 | D. | 升高温度(不考虑盐酸挥发) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 试剂 | 现象 | 结论 |
| A | 金属钠 | 有气体产生 | 含羟基或羧基或羟基、羧基 |
| B | 银氨溶液 | 产生银镜 | 含有醛基 |
| C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
| D | 溴水 | 溶液褪色 | 含有碳碳双键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
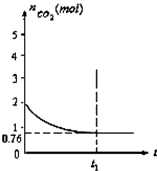 一定温度下2L的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应:
一定温度下2L的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,22.4LSO3所含的硫原子数目为NA | |
| B. | 常温常压下,7.8g过氧化钠含有的离子数为0.3NA | |
| C. | 18 g 水所含的电子数目为10 NA | |
| D. | 3.2g O2、O3混合物中所含氧原子一定是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 该反应中,热能转化为产物内部的能量 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H=-Q kJ/mol(Q>0) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com