
����Ŀ��25��ʱ��0.1mol Na2CO3�����������õ�һ�����Ϊ1L����Һ����Һ�в�������pH �Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ���ǣ� �� 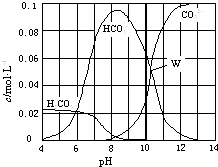
A.W����ʾ����Һ�У�c��CO32����=c��HCO3������c��OH������c��H+��
B.pH=4����Һ�У�c��H2CO3��+c��HCO3����+c��CO32����=0.1molL��1
C.pH=8����Һ�У�c��Na+����c��HCO3������c��H2CO3����c��CO32����
D.pH=11����Һ�У�c��Na+��+c ��H+��=c��OH����+c��Cl����+c��CO32����+c��HCO3����
���𰸡�AC
���������⣺A��W����ʾ����Һ��c��CO32����=c��HCO3��������Һ�Լ��ԣ���c��OH������c��H+����������Һ������Ũ�ȹ�ϵΪ��c��CO32����=c��HCO3������c��OH������c��H+������A��ȷ�� B��pH=4��˵����Ӧ����CO2���ɣ����Ը��������غ��֪c��H2CO3��+c��HCO3����+c��CO32������0.1 molL��1 �� ��B����
C������ͼ���֪pH=8ʱ����Һ��̼�����Ƶ�Ũ��ԶԶ����̼���Ƶ�Ũ�ȣ���˵����Ӧ��ǡ��������̼�����ƣ�HCO3����ˮ��̶ȴ��ڵ���̶ȣ���c��Na+����c��HCO3������c��H2CO3����c��CO32��������C��ȷ��
D������ͼ���֪pH=11ʱ����Һ̼���Ƶ�Ũ��ԶԶ����̼�����Ƶ�Ũ�ȣ���Һ�е���غ�Ϊ��c��Na+��+c ��H+��=c��OH����+c��Cl����+2c��CO32����+c��HCO3��������D����
��ѡAC��


 �ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
�ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͨ���û���Ӧ�õ�����������
A. Na��FeSO4��Һ���»�� B. COͨ�����ȵ�Fe2O3
C. H2ͨ��FeSO4��Һ D. Al��Fe3O4��ϼ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ� ��CH3OH��g��+H2O��g���TCO2��g��+3H2��g����H=+49.0kJmol��1
��CH3OH��g��+ ![]() O2��g���TCO2��g��+2H2��g����H=��192.9kJmol��1
O2��g���TCO2��g��+2H2��g����H=��192.9kJmol��1
����˵����ȷ���ǣ� ��
A.CH3OH��ȼ����Ϊ192.9 kJmol��1
B.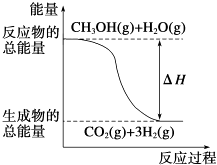 ��Ӧ���е������仯��ͼ��ʾ
��Ӧ���е������仯��ͼ��ʾ
C.CH3OHת���H2�Ĺ���һ��Ҫ��������
D.���ݢ���֪��ӦCH3OH��l��+ ![]() O2��g���TCO2��g��+2H2��g���ġ�H����192.9 kJmol��1
O2��g���TCO2��g��+2H2��g���ġ�H����192.9 kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200mL MgCl2�� AlCl3�Ļ����Һ������c��Mg2+��=0.2mol/L��c��Cl����=1.3mol/L��ҪʹMg2+ȫ��ת��Ϊ�������������������Ҫ2 mol/L NaOH ��Һ������ǣ� ��
A. 40mL B. 72 mL C. 80 mL D. 160mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����෨����ʶ���о���ѧ���ʳ��÷�����
��.�����������У���ˮ�� ���ռ� ���ۻ���KCl ���Ȼ��ƾ��� ������ ��̼�����ƹ��� ������ ������ ��Һ̬�Ȼ��� ������������Һ
��1���ܵ������_________�����ڵ���ʵ���__________�����ڷǵ���ʵ���________���������ڿո��У�
��2��д�����ʢ�����ˮ�ĵ��뷽��ʽ��____________________________��
��3�������ʢ����Ƴ���Һ����μ������Һ����������÷�Ӧ�����ӷ���ʽ��______________��
���������ʴ�������ת����ϵ��
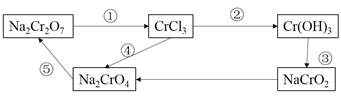
��1���������б�ŵIJ����У����û�ԭ������_____�����ţ���ͬ������������������___��
��2����ת����ϵ��֪Cr(OH)3Ϊ���������������д������KOH��Ӧ�����ӷ���ʽ��___________________________________________________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ij������ɫ��Ӧ�ʻ�ɫ���������п϶�������K+
B. ���˲���ʱ��Ϊ�˼ӿ���˿����ò���������©����Һ��
C. ����װ���У��¶ȼ�ˮ�����λ��Ӧ����������ƿ��֧�ܿڸ���
D. ���ε��ᴿʵ���У���Һ�������м��������ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ð�ˮ���������еĶ�����������ط�Ӧ����Ҫ�Ȼ�ѧ����ʽ���£� SO2��g��+NH3H2O��aq��=NH4HSO3��aq����H1=a kJmol��1
NH3H2O��aq��+NH4HSO3��aq��=��NH4��2SO3��aq��+H2O��l����H2=b kJmol��1
2��NH4��2SO3��aq��+O2��g��=2��NH4��2SO4��aq����H3=c kJmol��1
��1����Ӧ2SO2��g��+4NH3H2O��aq��+O2��g��=2��NH4��2SO4��aq��+2H2O��l���� ��H=kJmol��1 ��
��2������������NH4��2SO3���������¶ȵı仯��ͼ��ʾ�����¶ȳ���60��ʱ����NH4��2SO3���������½���ԭ������� ��
��3������ʯ�������̼���Ϊԭ���Ʊ�����泥���������˻������⣬��ʹ����Դ��ö������ã���Ӧ�����ӷ���ʽΪCaSO4��s��+CO32����aq��SO42����aq��+CaCO3��s�����÷�Ӧ��ƽ�ⳣ�� K= ��
[��֪Ksp��CaCO3��=2.9��10��9 �� Ksp��CaSO4��=9.1��10��6]
��4����NH4��2SO4�ڹ�ũҵ�������ж�����;�� �ٽ���ͭ������Ҫ�ɷ�Cu2S��������炙�Ϻ��ڿ����н��б��գ���ת��Ϊ����ͭͬʱ�����������÷�Ӧ�Ļ�ѧ����ʽΪ �� 
���о�����淋ķֽ���������ڶ���ʯ��Ŀ�������500��������立ֽ�����еõ�4�ֲ���京��������ʱ��仯��ϵ��ͼ����ʾ��д��������������立ֽ�Ļ�ѧ����ʽ�����õ����ű������ת�Ƶķ�����Ŀ�� ��
�ۣ�NH4��2SO4�ǹ�ҵ�Ʊ�K2SO4����Ҫԭ�ϣ�����ͼ����������ʵ��ܽ�����ߣ�������ҵ���Ʊ�K2SO4��������˼·�� �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����1mol H2��1mol Cl2��Ӧ����2mol HClʱ���ų�184.6kJ�������������۷���������ʵ���������в��죬��ͼ��ʾ������Ӧ�����仯�����۷���ʾ��ͼ��
��1����ѧ��������Ҫ����ͷš������ա���������
��2��ͼ�б�ʾ�����պ��ͷŵ������������ͷŵ�������kJ��
��3���÷�Ӧ�ķ�Ӧ���������������ڡ��������ڡ���С�ڡ�����Ӧ��������������Ը÷�Ӧ��������ȡ������ȡ�����Ӧ��
��4����ͼʾ���ݼ����䷴Ӧ�ȣ�д���÷�Ӧ���Ȼ�ѧ����ʽ 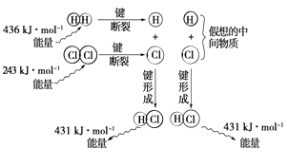
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2�������3 g������������ȼ�պ���150��ʱ���������ͨ��������Na2O2��Na2O2���ص�����Ϊ
A��1.5 g B��3 g C��6 g D��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com