
分析 A.单位时间内消耗2mol N2,同时生成4mol NH3,只能说明反应是正向进行;
B.单位时间内消耗3mol H2,同时生成2mol NH3,证明反应反应是正向进行;
C.单位时间内生成2mol N2,等效于消耗6molN-H键,同时形成6molN-H键;
D.混合气的密度ρ=$\frac{m}{V}$,m守恒,V不随时间而改变,所以密度始终不变;
E.前后气体系数和变化,所以容器中气体的压强不再随时间而改不变,证明达到了平衡;
解答 解:A、消耗2 mol N2的同时必生成4 mol NH3,故A不一定平衡,指明正反应方向;
B、单位时间内不论是否平衡,消耗3 mol H2的同时生成2 mol NH3,故无法判断是否达到平衡,指明正反应方向;
C、单位时间内生成2mol N2,等效于消耗6molN-H键,同时形成6molN-H键,说明反应已达平衡状态;
D、因为据ρ=m/V,气体的质量和体积不随反应是否进行而改变,即ρ始终是一个定值,故无法判断是否达到平衡;
E、因为反应如正向进行,压强p会减少,而p不再改变,说明反应已达平衡状态;故答案为:CE;ABD.
点评 本题考查了可逆反应的方向性及平衡状态标志的判断,注意知识的归纳和整理是解题的关键,难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y>X,离子半径:Z<W | |
| B. | 元素Y的单质能与元素X的最高价氧化物发生置换反应 | |
| C. | 元素Y和W能形成YW2型共价化合物 | |
| D. | W的单质有毒,且有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
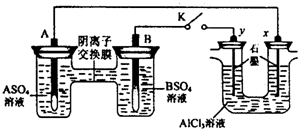 某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处
某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处| A. | 反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 | |
| B. | 溶液中(A2+)减小 | |
| C. | y电极上有H2产生,发生还原反应 | |
| D. | B的电极反应:B-2e═B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
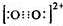 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石与碳纳米管互为同素异形体 | B. | N5与N2互为同素异形体 | ||
| C. | 14C的质子数为14 | D. | 乙醇和二甲醚属于同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
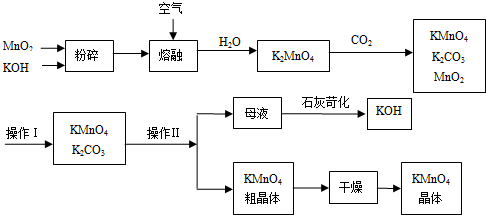
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com