
【题目】下列说法正确的是( )
A.5.6 g铁粉与硝酸反应失去电子数一定为0.3×6.02×1023
B.反应MgCl2(s)═Mg(s)+Cl2(g)的△H<0、△S>0
C.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关
D.0.1 mol?L﹣1 Na2SO3溶液中:c(OH﹣)﹣c(H+)=2c(H2SO3)+c(HS ![]() )
)
【答案】D
【解析】解:A、铁与硝酸反应生成物可能是Fe2+或Fe3+离子,当生成Fe2+离子时,转移的电子数为0.2×6.02×1023 , 当生成Fe3+离子时,转移的电子数为0.3×6.02×1023 , 故A错误; B、MgCl2的分解反应属于吸热反应,△H>0,反应后生成气体,熵变增加,△S>0,故B错误;
C、Ksp与为沉淀溶解平衡常数,只与难溶电解质的性质和温度有关,与溶液中相关离子的浓度无关,故C错误;
D、0.1molL﹣1Na2SO3溶液中,根据物料守恒有:c(Na+)=2c(H2SO3)+2c(HSO3﹣)+2c(SO32﹣),根据溶液电中性有:c(Na+)+c(H+)=c(HSO3﹣)+2c(SO32﹣)+c(OH﹣),则:c(OH﹣)﹣c(H+)=c(Na+)﹣c(HSO3﹣)﹣2c(SO32﹣)=2c(H2SO3)+2c(HSO3﹣)+2c(SO32﹣)﹣c(HSO3﹣)﹣2c(SO32﹣)=2c(H2SO3)+c(HSO3﹣),故D正确.
故选D.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 含有共价键的化合物一定是共价化合物
B. 只含有离子键的化合物才是离子化合物
C. 并非只有非金属原子间才能形成共价键
D. 由共价键形成的分子一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分.某化学兴趣小组为验证其组成元素,进行了如下实验:将少量样品放入A的燃烧管中,通入足量O2 , 用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置.(夹持仪器的装置已略去) 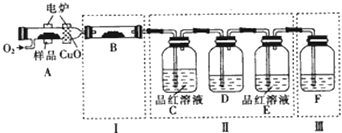
(1)写出A中样品燃烧的化学方程式: .
(2)装置B的目的是验证有机物中含氢元素,则B中盛装的试剂为 .
(3)D中盛放的试剂是(填字母). a.NaOH溶液 b.品红溶液 c.KMnO4溶液 d.饱和石灰水
(4)能证明有机物含碳元素的现象是 .
(5)燃烧管中放入CuO的作用是 .
(6)请指出装置F中的错误: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中,共价键被破坏的是( )
①碘升华 ②HCl气体溶于水 ③NH4Cl受热分解 ④氧氧化钠熔化
A. ①② B. ②③ C. ②③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和联氨(N2H4)既是一种工业原料,又是一种重要的工业产品.
(1)实验室可用氯化铵与消石灰反应制取氨气,其反应的化学方程式为 .
(2)联氨在一定条件下可按下式分解:3N2H4(g)=N2(g)+4NH3(g),已知断裂1molN﹣H、N﹣N及N≡N需吸收的能量依次为390.8kJ、193kJ、946kJ.若生成1molN2 , 则反应(填“放出”或“吸收”)kJ的能量.
(3)NH3﹣O2燃料电池的结构如图所示. 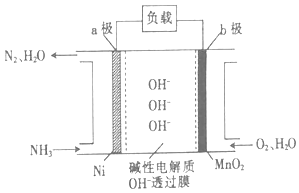
①a极为电池的(填“正”或“负”)极.
②当生成1molN2时,电路中流过电子的物质的量为 .
(4)联氨可以高效地脱除烟道气中的NO从而生成N2 , 该反应中氧化产物与还原产物的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有0.4g铁的氧化物,用足量的CO在高温下将其还原,把生成的CO2全部通入足量澄清石灰水中,得到0.75g沉淀.这种铁的氧化物的化学式是( )
A.FeO
B.Fe2O3
C.Fe3O4
D.FeO和Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示: 
(1)请列举海水淡化的一种方法 .
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、、 .
(3)步骤Ⅰ中已经获得Br2 , 步骤Ⅱ中又将获得的Br2还原为Br﹣ , 其目的是
(4)步骤Ⅱ用SO2水溶液吸收Br2 , 吸收率可达95%,该反应的离子方程式为 . 由此反应可知,除保护环境外,在工业生产中还应解决的问题是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南海争端、南海仲裁案一直牵动国人的心,南海是一个巨大的资源宝库,海水开发利用的部分过程如下图所示.下列有关说法正确的是( ) 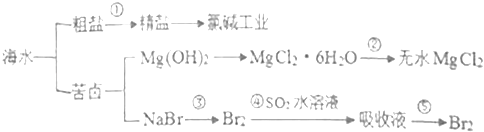
A.第①步中除去粗盐中的SO42﹣、Ca2+、Mg2+等杂质,加入药品的顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液、过滤后加盐酸
B.第②步的关键要低温小火烘干
C.氯碱工业的阴极产物是Cl2
D.第③步到第⑤步的目的是为了富集溴元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对原子核外电子以及电子的运动,下列描述正确的是( ) ①可以测定某一时刻电子在原子中所处的位置
②电子质量很小且带负电荷
③电子在原子里有“广阔”的运动空间
④运动速度接近光速
⑤与宏观物体一样有固定的运动轨道
⑥现代最先进的扫描隧道显微镜也观察不到电子的运动.
A.①②③⑥
B.②③④⑥
C.③④⑤⑥
D.⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com