

 .
. .
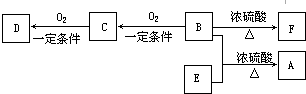
. 分析 (1)浓硫酸增重为水的质量,碱石灰增重为二氧化碳的质量,以此可确定有机物中C、H原子个数比值,结合消耗氧气的体积可确定有机物中各原子个数比值;
(2)根据有机物原子个数比值可确定最简式,结合相对分子质量可确定有机物分子式;
(3)根据有机物分子式结合价键理论可确定有机物的可能结构;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,二甲醚只有一种不同化学环境的氢原子;
(5)A为乙醇在一定条件下脱水可生成B为乙烯,乙烯可合成包装塑料C为聚乙烯;
(6)用B选择合适的方法制备氯乙烷,要求原子利用率为100%,是利用乙烯和氯化氢加成反应得到氯乙烷;
(7)反应为乙酸与乙醇的酯化反应.
解答 解:(1)由题意可知n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,n(O2)=$\frac{0.67L}{22.4L/mol}$=0.3mol,
根据氧原子守恒可知有机物中含有n(O)=0.3mol+0.2mol×2-0.3mol×2=0.1mol,
则有机物中N(C):N(H):N(O)=0.2mol:0.6mol:0.1mol=2:6:1,
故答案为:2:6:1;
(2)该物质中各元素的原子个数比为N(C):N(H):N(O)=2:6:1,则最简式为C2H6O,其相对分子质量为46,则有机物的分子式为C2H6O,
故答案为:C2H6O;
(3)有机物的分子式为C2H6O,分子中可能存在C-C、C-H、C-O、O-H等化学键,可能的结构简式有CH3CH2OH或CH3OCH3,
故答案为:CH3CH2OH或CH3OCH3.
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即CH3CH2OH,二甲醚只有一种不同化学环境的氢原子,
故答案为:CH3CH2OH;
(5)A为乙醇在一定条件下脱水可生成B为乙烯,乙烯可合成包装塑料C为聚乙烯,反应的化学方程式为: ,
,
故答案为: ;
;
(6)用B选择合适的方法制备氯乙烷,要求原子利用率为100%,是利用乙烯和氯化氢加成反应得到氯乙烷,反应的化学方程式为:nCH2=CH2+HCl $\stackrel{催化剂}{→}$ CH3CH2Cl,
故答案为:nCH2=CH2+HCl $\stackrel{催化剂}{→}$ CH3CH2Cl;
(7)发生一系列的化学变化而变得更醇香,应为乙醇被氧化为乙酸,进而发生酯化反应生成乙酸乙酯,反应的方程式为 ,
,
故答案为: ;
;
点评 本题考查有机物的推断,题目难度不大,本题注意从质量守恒的角度判断有机物最简式,是解答该题的关键.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
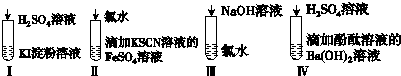
| 选项 | 现象 | 离子方程式 |
| A | I在空气中放置一段时间后,溶液呈蓝色 | 4I-+O2+2H2O═2I2+4OH- |
| B | II溶液由浅绿色变为红色 | Fe2++Cl2═Fe3++2Cl- Fe3++3SCN-═Fe(SCN)3 |
| C | III溶液 颜色无变化 | Cl2+2OH-═Cl-+ClO-+H2O |
| D | IV有白色沉淀生成,溶液由红色变无色 | Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、水泥、水晶都是硅酸盐制品 | |
| B. | 将秸秆焚烧可得富含钾肥的草木灰,焚烧是一种较为理想的秸秆处理办法 | |
| C. | 石油的分馏和煤的气化、液化,涉及的都是物理变化 | |
| D. | 纤维素不能被人体消化吸收,但能促进肠道的蠕动,对人体有益 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
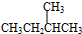 与
与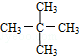 G.
G.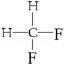 与
与 
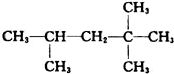 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:CH3C(CH3)2C(CH3)2CH3;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:CH3C(CH3)2C(CH3)2CH3;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为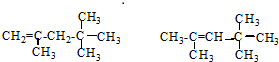 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:实验题
A.移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞 |
B.用标准溶液润洗滴定管2-3次 |
C.把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液 |
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm |
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)B-
(2)滴定开始后,眼睛注视 ,判断到达终点的现象是 。
(3)下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
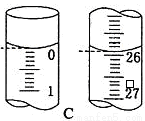
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com