
在3H2(g)+N2(g)  2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
A. 1s B. 0.44s C. 1.33s D. 2s
科目:高中化学 来源: 题型:
A.通入He保持压强不变 B.通入H2而容积不变
C.通入He而容积不变 D.通入N2而容积不变
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市房山区房山中学高二下学期期中考试化学试卷(带解析) 题型:填空题
氨气是生产化肥、硝酸的重要原料,围绕合成氨人们进行了一系列的研究
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH =" -483.6" kJ/mol
3H2 (g) + N2 (g)  2NH3 (g) ΔH =" -92.4" kJ/mol
2NH3 (g) ΔH =" -92.4" kJ/mol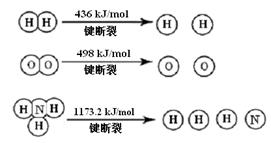
计算断裂1 mol N≡N键需要能量 kJ , 氮气分子中化学键比氧气分子中的 化学键键 (填“强”或“弱”),
(2)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:
N2 (g) + O2 (g) =" 2NO" (g) ΔH =" +180.8" kJ/mol ,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是 。
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
 2NH3 (g)测得甲容器中H2的转化率为40%。
2NH3 (g)测得甲容器中H2的转化率为40%。| | N2 | H2 | NH3 |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1.5 | 1 |
| 丙 | 0 | 0 | 4 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市丰台区高三上学期期末考试化学试卷(解析版) 题型:填空题
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH = -483.6 kJ/mol
3H2 (g) + N2 (g)  2NH3 (g) ΔH =
-92.4 kJ/mol
2NH3 (g) ΔH =
-92.4 kJ/mol
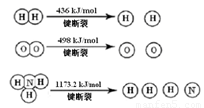
计算断裂1 mol N≡N键需要能量 kJ , 氮气分子中化学键比氧气分子中的化学键键 (填“强”或“弱”),因此氢气与二者反应的条件不同。
(2)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:N2 (g) + O2 (g) = 2NO (g) ΔH = +180.8 kJ/mol ,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是 。
|
反应 |
大气固氮 |
工业固氮 |
||||
|
温度/℃ |
27 |
2000 |
25 |
350 |
400 |
450 |
|
K |
3.84×10-31 |
0.1 |
5×108 |
1.847 |
0.507 |
0.152 |
A.常温下,大气固氮几乎不可能进行,而工业固氮非常容易进行
B.人类大规模模拟大气固氮是无意义的
C.工业固氮温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大
(3)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料, 发生反应:3H2
(g) + N2 (g)  2NH3
(g)测得甲容器中H2的转化率为40%。
2NH3
(g)测得甲容器中H2的转化率为40%。
|
|
N2 |
H2 |
NH3 |
|
甲 |
1 |
3 |
0 |
|
乙 |
0.5 |
1.5 |
1 |
|
丙 |
0 |
0 |
4 |
判断乙容器中反应进行的方向 。(填“正向”或“逆向”)
达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为 。
(4)氨气是合成硝酸的原料,写出氨气与氧气反应生成一氧化氮和气态水的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在3H2(g)+N2(g) 2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
A. 1s B.0.44s C. 1.33s D. 2s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com