
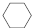
 (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$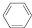 (g)+3H2(g).
(g)+3H2(g).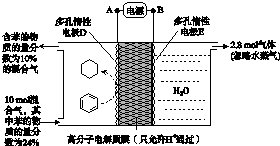
分析 (1)n(H2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,根据方程式2Li+H2$\frac{\underline{\;\;△\;\;}}{\;}$2LiH知,0.5mol氢气参加反应生成1molLiH,m(LiH)=1mol×7g/mol=7g,V(LiH)=$\frac{m}{ρ}$;
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,还生成氢气,且反应前后B的化合价不变,可知H元素化合价由-1价、+1价变为0价,再结合转移电子守恒书写化学方程式;
(3)释放出的H2 包括Mg17Al12吸收的氢,还包括镁、铝和盐酸反应生成的氢气;
(4) (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)
开始(mol)a 0 0
反应(mol)b b 3b
平衡(mol)a-b b 3b
平衡时同一容器中各物质的压强之比等于其物质的量之比,所以环己烷的分压=$\frac{a-b}{a+3b}$PMpa,苯的分压=$\frac{b}{a+3b}$PMpa、氢气的分压=$\frac{3b}{a+3b}$PMpa,化学平衡常数Kp等于生成物浓度压强的幂之积与反应物分压的幂之积的比;
(5)①根据图知,D电极上苯生成环己烷,该电极上得电子发生还原反应,所以D为阴极、E为阳极,所以A是负极、B是正极,导线中电流从正极流向阳极;
②该实验目的是储氢,阴极上苯得电子和氢离子反应生成环己烷而储氢.
解答 解:(1)n(H2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,根据方程式2Li+H2$\frac{\underline{\;\;△\;\;}}{\;}$2LiH知,0.5mol氢气参加反应生成1molLiH,m(LiH)=1mol×8g/mol=8g,V(LiH)=$\frac{m}{ρ}$=$\frac{8g}{0.8g/mL}$=0.01L,所以LiH与氢气的体积之比=0.01L:11.2L=$\frac{1}{1120}$,
故答案为:$\frac{1}{1120}$;
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,还生成氢气,且反应前后B的化合价不变,所以NaBH4与H2O中H元素发生归中反应,H元素化合价由-1价、+1价变为0价,依据得失电子守恒可知:NaBH4的系数为1,H2O的系数为2,依据原子个数守恒配平反应方程式:NaBH4+2H2O=NaBO2+4H2↑,
故答案为:NaBH4+2H2O=NaBO2+4H2↑;
(3)1molMg17Al12完全吸氢17mol,在盐酸中会全部释放出来,镁铝合金中的镁和铝都能与盐酸反应生成H2,生成氢气的物质的量分别为17mol、18mol,则生成氢气一共(17+17+12×$\frac{3}{2}$)mol=52mol,
故答案为:52mol;
(4) (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)
开始(mol)a 0 0
反应(mol)b b 3b
平衡(mol)a-b b 3b
平衡时同一容器中各物质的压强之比等于其物质的量之比,所以环己烷的分压=$\frac{a-b}{a+3b}$PMpa,苯的分压=$\frac{b}{a+3b}$PMpa、氢气的分压=$\frac{3b}{a+3b}$PMpa,
化学平衡常数Kp=$\frac{(\frac{b}{a+3b}PMPa).(\frac{3b}{a+3b}PMPa)^{3}}{\frac{a-b}{a+3b}PMPa}$=$\frac{27{b}^{4}{P}^{3}}{(a-b)(a+3b)^{3}}(MPa)^{3}$,
故答案为:$\frac{27{b}^{4}{P}^{3}}{(a-b)(a+3b)^{3}}(MPa)^{3}$;
(5)①根据图知,D电极上苯生成环己烷,该电极上得电子发生还原反应,所以D为阴极、E为阳极,所以A是负极、B是正极,导线中电流从正极流向阳极,即电流从B流向E,故答案为:B→E;
②该实验目的是储氢,阴极上苯得电子和氢离子反应生成环己烷而储氢,电极反应式为C6H6+6H++6e-═C6H12,
故答案为:C6H6+6H++6e-═C6H12.
点评 本题考查较综合,涉及化学平衡计算、电解原理等知识点,侧重考查学生分析计算及知识迁移能力,把握化学反应原理是解本题关键,注意平衡常数Kp表达式的书写,题目难度中等.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是
A.单质都是由同种元素组成的,只含一种元素的物质一定是纯净物
B.金属铝排在金属活动性顺序表中氢元素的前面,铝与酸反应一定放出氢气
C.中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应
D.氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
关于酸、碱、盐的下列各种说法中,正确的是
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl通电时能电离出NH4+和Cl?,所以NH4Cl是盐
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
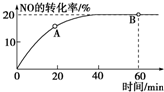 (1)某温度下,向容积为1L的容器中充入3mol NO和1mol CO,发生2NO(g)+2CO(g)???N2(g)+2CO2(g)反应,NO的转化率随时间的变化如图所示.
(1)某温度下,向容积为1L的容器中充入3mol NO和1mol CO,发生2NO(g)+2CO(g)???N2(g)+2CO2(g)反应,NO的转化率随时间的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
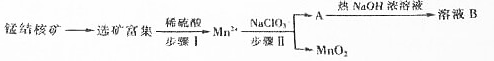
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
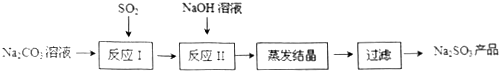
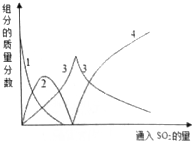
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
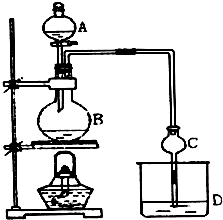 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 开始沉淀 | 完全沉淀 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| Al(OH)3 | 3.7 | 5.7 |
| 开始溶解:7.8 | 完全溶解:10.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com