
 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
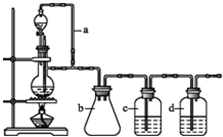
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:分析 (1)制备氢气选用锌粒和稀盐酸;制备丙烯选用2-丙醇和浓硫酸;
(2)在题给装置中,a的作用保持分液漏斗和烧瓶内的气压相等,以保证分液漏斗内的液体能顺利加入烧瓶中;b主要是起安全瓶的作用,以防止倒吸;
(3)若用题给装置制备H2,则不需要酒精灯,c为除去氢气中的酸性气体,选用NaOH溶液,d为除去氢气中的H2O,试剂选用浓硫酸;
(4)检验丙烯和少量SO2、CO2及水蒸气组成的混合气体各成分时,应首先选④无水CuSO4检验水蒸气,然后用②品红溶液检验SO2,并用①饱和Na2SO3溶液除去SO2;然后用②品红溶液检验SO2是否除尽,然后用③石灰水检验CO2,用⑤酸性KMnO4溶液检验丙烯;
(5)加饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开.
解答 解:(1)氢气可用活泼金属锌与非氧化性酸盐酸通过置换反应制备,氧化性酸如硝酸和浓硫酸与锌反应不能产生氢气,方程式为Zn+2HCl=ZnCl2+H2↑;
2-丙醇通过消去反应即到达丙烯,反应的方程式为:(CH3)2CHOH$→_{△}^{浓硫酸}$CH2=CHCH3↑+H2O,
故答案为:Zn+2HCl=ZnCl2+H2↑; (CH3)2CHOH$→_{△}^{浓硫酸}$CH2=CHCH3↑+H2O;
(2)甲酸在浓硫酸的作用下通过加热脱水生成CO,为了使产生的气体能顺利的从发生装置中排出,就必需保持压强一致,因此a的作用是保持恒压,保证分液漏斗内外压强平衡,便于液体顺利流下;
由于甲酸易挥发,产生的CO中必然混有甲酸,所以在收集之前需要除去甲酸,可以利用NaOH溶液吸收甲酸.又因为甲酸易溶于水,所以必需防止液体倒吸,即b的作用是作安全瓶,防倒吸
故答案为:平衡分液漏斗液面压强与圆底烧瓶内压强;防倒吸;
(3)若用以上装置制备氢气,就不再需要加热,产生的氢气中必然会混有氯化氢,所以在收集之前需要除去氯化氢,可以利用NaOH溶液吸收氯化氢,d为除去氢气中的H2O,试剂选用浓硫酸,
故答案为:NaOH溶液;浓硫酸;
(4)检验丙烯可以用酸性KMnO4溶液,检验SO2可以用酸性KMnO4溶液、品红溶液或石灰水,检验CO2可以用石灰水,检验水蒸气可以用无水CuSO4,所以在检验这四种气体时必需考虑试剂的选择和顺序.只要通过溶液,就会产生水蒸气,因此先检验水蒸气,然后检验SO2并在检验之后除去SO2,除SO2可以用饱和Na2SO3溶液,最后检验CO2和丙烯,因此顺序为④②①②③⑤(或④②①③⑤),
故答案为:④②①②③⑤(④②①③⑤);
(5)粗品中含有正丁醛,根据所给的信息利用加饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;由于饱和NaHSO3溶液是过量的,所以加入乙醚的目的是萃取溶液中的1-丁醇.因为1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开,
故答案为:饱和NaHSO3溶液;过滤;萃取;蒸馏.
点评 本题考查有机物合成方案的设计,题目难度较大,综合性较强,答题时注意把握物质的分离、提纯方法,把握物质的性质的异同是解答该题的关键,试题培养了学生的分析、理解能力及化学实验能力.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2 Na2O2+2H2O═4NaOH+O2↑ | B. | 2 Na+2H2O═2NaOH+H2↑ | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$ 2H2O | D. | HCl+NH3═NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若△H>0,△S>0,低温时可自发进行 | |
| B. | 若△H<0,△S<0,低温时可自发进行 | |
| C. | 若△H<0,△S>0,任何温度下都能自发进行 | |
| D. | 若△H>0,△S<0,任何温度下都不能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v正(N2)=v逆(NH3) | B. | v正(N2)=3v正(H2) | ||
| C. | v正(H2)=$\frac{3}{2}$ v逆(NH3) | D. | N2、H2、NH3的体积比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
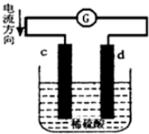 将铜片、锌片插入500mL2mol/L稀硫酸中组成原电池,c、d为两个电极.则下列有关的判断正确的是(溶液体积变化忽略不计)( )
将铜片、锌片插入500mL2mol/L稀硫酸中组成原电池,c、d为两个电极.则下列有关的判断正确的是(溶液体积变化忽略不计)( )| A. | c为负极,其质量逐渐减小,发生还原反应 | |
| B. | 当有0.2mol电子通过电路,正极表明产生气体2.24L | |
| C. | 电池工作的过程中,溶液中SO42-浓度逐渐减小 | |
| D. | 当负极质量减轻32.5g时,烧杯中溶液中H+的浓度为2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 奥运火炬燃烧主要是将化学能转变为热能和光能 | |
| B. | 丙烷常温下是液体 | |
| C. | 丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极 | |
| D. | 丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸锌溶液 | B. | 氢氧化钠固体 | C. | 碳酸钠固体 | D. | 硫酸铜固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com