
����β����NOx�����������������������㷺��ע��
��1��ij��ȤС����������������Ϣ��
N2(g)+O2(g)=2NO(g) ��H=+180.5kJ/mol
2H2(g)+O2(g)=2H2O(g)) ��H=�D483.6kJ/mol
��Ӧ2H2(g)+2NO(g)=2H2O(g)+N2(g) ��H= ��
��2����С�����õ��ԭ���������ͼ1װ�ý���H2��ԭNO��ʵ��[�����ӵ����Ե�SCY�մ�(�ܴ���H+)Ϊ���ʣ������ٱ�Ĥ���缫]��
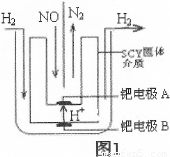
�ٵ缫AΪ �����缫��ӦʽΪ ��
��3����������ԭNOԭ�����£�
����Ӧ��4NO(g)+4NH3(g)+O2(g)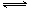 4N2(g)+6H2O(g)
(��H <0)
4N2(g)+6H2O(g)
(��H <0)
����Ӧ��4NH3(g)+3O2(g)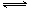 2N2(g)+6H2O(g)
2N2(g)+6H2O(g)
4NH3(g)+ 4O2(g)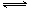 2N2O(g)+6H2O(g)
2N2O(g)+6H2O(g)
4NO(g)+4NH3(g)+3O2(g) 4N2O(g)+6H2O(g)
4N2O(g)+6H2O(g)
�й�ʵ�������ͼ2��ͼ3��ʾ���ݴ˻ش��������⣺

�ٴ���ԭNOӦ����n(NH3)/n(NO)�����ֵΪ �������� ��
������Ӧƽ�ⳣ������ʽ��K= �������¶ȵ����ӣ�K�� (ѡ����ӡ��� ����С�����䡱��
��Ӱ��N2O�����ʵ������� ������Ũ�Ⱥ� ��
��1���D664.1kJ/mol (2��)
��2������(2��) 2NO+4H++4e��=N2��+2H2O (2��)
��3����1 (1��) n(NH3)/n(NO)С��1ʱ��NO�ѳ��ʲ��ߣ�n(NH3)/n(NO)����1ʱ��NO�ѳ������Ӳ�������N2O�������������ӣ� 3�֣�
��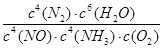 (2��)
��С(2��)
(2��)
��С(2��)
���¶�(1��) n(NH3)/n(NO) (1��)(�������մ�˳��ɵߵ�)
��������
�����������1�����ݸ�˹���ɣ�����2����Ӧ��ȥ��1����Ӧ�ɵã���H=�D664.1kJ/mol����2����ԭ���ԭ����֪���ڵ�·��������������������ͼ��֪���ٵ缫AΪ�������ٵ缫BΪ�������ɵ��ӡ���ɡ�ԭ�Ӿ��غ��֪�����Ի��������������Ļ�ԭ��ӦʽΪ2NO+4H++4e��=N2��+2H2O����3���ٶ�ͼ���Աȿ�֪��n(NH3)/n(NO)С��1ʱ��NO�ѳ��ʲ��ߣ�n(NH3)/n(NO)����1ʱ��NO�ѳ������Ӳ�������N2O�������������ӣ����n(NH3)/n(NO)�����ֵΪ1�����ɷ�Ӧʽ��֪��K=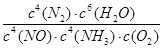 �����ڡ�H<0������Ӧ���ȣ�����ƽ�����ƣ�K��С�����������Ϣ��֪��Ӱ��N2O�����ʵ��������¶ȡ�n(NH3)/n(NO)
������Ũ�ȡ�
�����ڡ�H<0������Ӧ���ȣ�����ƽ�����ƣ�K��С�����������Ϣ��֪��Ӱ��N2O�����ʵ��������¶ȡ�n(NH3)/n(NO)
������Ũ�ȡ�
���㣺�����˹���ɡ�ԭ��ء���ѧƽ������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �� |
| ||
| ||

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���Ĵ�ʡ��֦���и����ڶ���ͳ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�о��������������PM2.5�ȴ�����Ⱦ�������������Ҫ���塣
��1����PM2.5����������ˮ�����Ƴɴ�������������ø������г�H+��OH��������ˮ�������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
|
���� |
K+ |
Na+ |
NH4+ |
SO42- |
NO3�� |
Cl�� |
|
Ũ��/mol��L-1 |
4��10-6 |
6��10-6 |
2��10-5 |
4��10-5 |
3��10-5 |
2��10-5 |
���ݱ��������ж�������pH =
��2����SO2�Ĺ�ҵ���������������Ľ�����SO2�ķ���ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ��������ڷ�������Ĺ����У����õ�ʯ��ʯ��Һ�ڽ�������װ��ǰ����ͨһ��ʱ��Ķ�����̼��������������Ч�ʣ�����ʱ���ƽ�Һ��pHֵ����ʱ��Һ���е���������ƿ��Ա���������������������ơ�
������̼��ʯ��ʯ��Һ��Ӧ�õ��IJ���Ϊ ��
��������Ʊ���������������������ƵĻ�ѧ����ʽΪ ��
��3������β����NOx��CO�����ɼ�ת����
����֪����������NO�ķ�ӦΪ��N2(g)+O2(g�� 2NO(g��
2NO(g��  H��0
H��0
���������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��
��������β��ϵͳ�а�װ��ת������ʹNO��COѸ�ٷ�����Ӧת���ɶԻ�������Ⱦ�����壬�ɼ���CO��NO����Ⱦ����Ӧ�Ļ�ѧ����ʽΪ ��
��4����CH4����ԭNOx�������������������Ⱦ�����磺
CH4(g)��4NO2(g���� 4NO(g)��CO2(g)��2H2O(g����H����574kJ��mol��1
CH4(g)��4NO(g���� 2N2(g)��CO2(g)��2H2O(g����H����1160kJ��mol��1
H2O(g���� H2O(l����H����144kJ��mol��1
ȡ��״����4.48LCH4��ԭNO2��NO�Ļ���������������ȫ����ԭ��������H2O(l)����ų���������Q��ȡֵ��Χ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 O+O2
O+O2 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ������
 O��O2 ��NO��O3��NO2��O2 ��NO2��O��NO��O2
O��O2 ��NO��O3��NO2��O2 ��NO2��O��NO��O2 

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com