
硫、氮、稀土元素的单质和化合物应用广泛。
Ⅰ.(1)将硫铁矿和焦炭放在炼硫炉中,在有限空气中燃烧,发生下列反应:
3FeS2 + 12 C + 8O2 = Fe3O4 + 12CO + 6S
生成3mol硫时,被氧化的物质物质的量为__ _________。
(2)过硫酸钾化学式为:K2S2O8,过硫酸结构式为
①过硫酸钾和过硫酸均有强氧化性,不稳定,容易分解,如2H2S2O8=2H2SO4+2SO3+O2
下列能加快过硫酸分解的固体物质是 。
A.CuO B.MnO2 C.Fe2O3 D.NaNO3
②已知硫酸锰(MnSO4)和过硫酸钾两种盐溶液在催化剂存在下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。请写出上述反应的化学方程式:____________ __________。
③若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_________________。
Ⅱ.稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,由CeCl3·6H2O制备无水CeCl3应采取的措施是 _ _。
Ⅰ.(1)7.5mol (2分)
(2)①ABC(全对给2分,有错0分,缺项但无错给1分)
②8H2O + 2MnSO4 + 5K2S2O8 = 2KMnO4 + 4K2SO4 + 8H2SO4(2分,不配平或化学式出现错误均为0分,写离子方程式完全正确给1分,有错0分)
③氯气(2分)(分子式、名称均可)
Ⅱ.在通入氯化氢气体的条件下加热除去结晶水(2分)
【解析】
试题分析:Ⅰ.(1)从化学方程式可看出Fe、S、C三种元素的化合价均升高,所以被氧化的物质为FeS2和C,生成3mol硫时,被氧化的FeS2为1.5mol,被氧化的C为6mol硫,共7.5mol。(2) ①类比CuO、MnO2、Fe2O3对过氧化氢分解的催化作用可做出判断;②反应后生成H2SO4说明有水参加反应,根据化合价变化情况配平后即得化学方程式:8H2O + 2MnSO4 + 5K2S2O8 = 2KMnO4 + 4K2SO4 + 8H2SO4;③K2S2O8 氧化性比KMnO4强,可把Cl–氧化为氯气,故生成物还有氯气。Ⅱ.为抑制CeCl3水解,CeCl3·6H2O应在氯化氢气氛中加热除去结晶水制备无水CeCl3。
考点:主要考查氧化还原反应及其配平、化学方程式的书写、盐的水解,考查综合分析能力。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:阅读理解


| 2aV1-bV2 |
| 2000 |
| 2aV1-bV2 |
| 2000 |
| 0.01mol?L-1 KIO3酸性溶液(含淀粉)的体积/mL |
0.01mol?L-1 Na2SO3溶液的体积/mL |
H2O的体积 /mL |
实验 温度 /℃ |
溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| aV1-0.5bV 2 |
| 1000 |
| aV1-0.5bV 2 |
| 1000 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
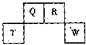 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
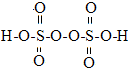
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com