
| A. | 根据分散系是否有丁达尔现象,将分散系分为胶体、浊液和溶液 | |
| B. | 用盐酸可以清洗长期存放过FeCl3溶液的试剂瓶 | |
| C. | 二氧化硅广泛用于制作计算机芯片和光导纤维 | |
| D. | 电解精炼铜时,阳极泥中含有Fe、Ag、Au等金属 |
分析 A.胶体、浊液和溶液的本质区别是分散质微粒大小;
B.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁;
C.计算机芯片的主要成分是硅单质;
D.电解精炼铜,阳极上的铁也会失电子生成离子,阳极泥是银、金等.
解答 解:A.根据分散系分散质微粒大小将分散系分为溶液、胶体和浊液,故A错误;
B.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁,可与盐酸反应,故B正确;
C.计算机芯片的主要成分是硅单质,光导纤维的主要成分是二氧化硅,故C错误;
D.电解精炼铜,阳极上的铁也会失电子生成离子,阳极泥是银、金等,故D错误;
故选B.
点评 本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,题目贴近高考,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 气体的体积和体系的压强 | B. | 溶液颜色的深浅 | ||
| C. | 固体物质的体积 | D. | H+浓度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
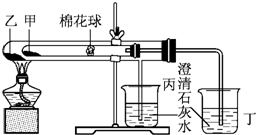 下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察下图的实验装置,分析实验原理,回答下列问题:
下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察下图的实验装置,分析实验原理,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4分子的比例模型: | B. | 氯原子的结构示意图: | ||
| C. | NH3分子的电子式: | D. | CO2分子的结构式:O=C=O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
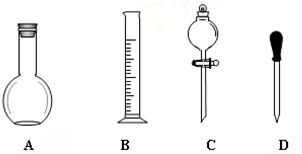 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有两研究性学习小组拟探究卤代烃的性质.查资料得知:溴乙烷的沸点为3.4℃,乙醇的沸点℃.
有两研究性学习小组拟探究卤代烃的性质.查资料得知:溴乙烷的沸点为3.4℃,乙醇的沸点℃.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制氯气,是在加热条件下,二氧化锰固体与稀盐酸反应 | |
| B. | 新制氯水中只含有Cl2和H2O分子 | |
| C. | 随着氯元素化合价的升高,氯的含氧酸的酸性逐渐增强 | |
| D. | 氯气可用作消毒剂和漂白剂,是因为氯气分子具有强的氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com