
 .
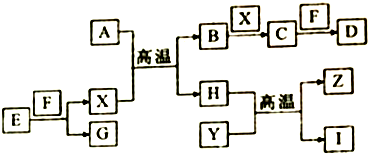
.分析 A为某种矿石的主要成分,只含有两种元素且元素的质量比为7:8,Y、Z是常见的金属单质,常温下Y、Z在D的浓溶液中发生钝化,则Y、Z为Al或Fe,D为硫酸或硝酸,Y高温下反应生成Z,则Y为Al,Z为Fe,该反应为铝热反应,所以H为铁的氧化物,I为氧化铝,F是最常见的无色液体,则F为H2O,E是一种淡黄色固体,E能与F反应生成X和G,则E为Na2O2,X为气体单质,则X为O2,所以G为NaOH,B是形成酸雨的主要因素,则B为SO2,SO2与氧气反应生成C为SO3,C与水反应生成D为H2SO4,根据元素守恒可知,A中含有铁元素和硫元素,A为某种矿石的主要成分,只含有两种元素且元素的质量比为7:8,则A为FeS2,据此答题.
解答 解:A为某种矿石的主要成分,只含有两种元素且元素的质量比为7:8,Y、Z是常见的金属单质,常温下Y、Z在D的浓溶液中发生钝化,则Y、Z为Al或Fe,D为硫酸或硝酸,Y高温下反应生成Z,则Y为Al,Z为Fe,该反应为铝热反应,所以H为铁的氧化物,I为氧化铝,F是最常见的无色液体,则F为H2O,E是一种淡黄色固体,E能与F反应生成X和G,则E为Na2O2,X为气体单质,则X为O2,所以G为NaOH,B是形成酸雨的主要因素,则B为SO2,SO2与氧气反应生成C为SO3,C与水反应生成D为H2SO4,根据元素守恒可知,A中含有铁元素和硫元素,A为某种矿石的主要成分,只含有两种元素且元素的质量比为7:8,则A为FeS2,
(1)F为H2O,F的电子式为 ,
,
故答案为: ;
;
(2)A为FeS2,
故答案为:FeS2;
(3)E为Na2O2,过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(4)Z为Fe,铁与稀硫酸反应的离子方程式为2H++Fe=H2↑+Fe2+,
故答案为:2H++Fe=H2↑+Fe2+.
点评 本题考查了物质转化关系的分析判断,物质性质的应用,反应现象和反应条件的应用是解题关键,主要考查过氧化钠的性质、铁及其化合物性质的应用,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
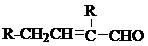
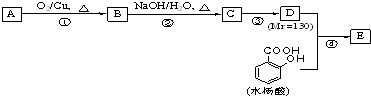
 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 (其中两种).
(其中两种). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
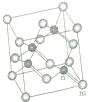 第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.
第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.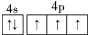 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰 | B. | 还原铁粉 | C. | 氯化钙 | D. | 硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前者多 | B. | 后者多 | C. | 一样多 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl | B. | FeCl2 | C. | KOH | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
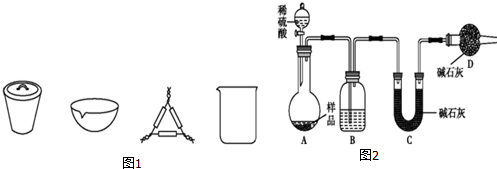
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com