

 £¬
£¬·ÖĪö ³£ĪĀĻĀAĪŖ¹ĢĢåµ„ÖŹ£¬BĪŖµ»ĘÉ«·ŪÄ©£¬CŹĒĘųĢ壬AŗĶC·“Ӧɜ³ÉB£¬ŌņBŹĒNa2O2£¬AŹĒNa£¬CŹĒO2£»EŌŚ³£ĪĀĻĀĪŖŅŗĢ壬EŹĒH2O£¬ÄĘŗĶĖ®·“Ӧɜ³ÉNaOHŗĶĒāĘų£¬¹żŃõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£¬CŹĒŃõĘų£¬DŹĒNaOH£¬FŹĒH2£»HµÄĖ®ČÜŅŗĶصēÉś³ÉĒāĘų”¢IĘųĢåŗĶĒāŃõ»ÆÄĘ£¬ĒŅJæÉ×÷ɱ¾śĻū¶¾¼Į£¬ĪŖ“ĪĀČĖįŃĪ£¬ĖłŅŌIŹĒCl2£¬µē½ā±„ŗĶŹ³ŃĪĖ®ÖĘČ”ĀČĘų£¬ĖłŅŌHŹĒNaCl£¬ĒāĘųŗĶĀČĘų·“Ӧɜ³ÉG£¬ĖłŅŌGŹĒHCl£»ĀČĘųŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬ĖłŅŌJŹĒNaClO£¬Č»ŗó½įŗĻĪļÖŹµÄŠŌÖŹ¼°»ÆѧÓĆÓļĄ“½ā“š£®
½ā“š ½ā£ŗ³£ĪĀĻĀAĪŖ¹ĢĢåµ„ÖŹ£¬BĪŖµ»ĘÉ«·ŪÄ©£¬CŹĒĘųĢ壬AŗĶC·“Ӧɜ³ÉB£¬ŌņBŹĒNa2O2£¬AŹĒNa£¬CŹĒO2£»EŌŚ³£ĪĀĻĀĪŖŅŗĢ壬EŹĒH2O£¬ÄĘŗĶĖ®·“Ӧɜ³ÉNaOHŗĶĒāĘų£¬¹żŃõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£¬CŹĒŃõĘų£¬DŹĒNaOH£¬FŹĒH2£»HµÄĖ®ČÜŅŗĶصēÉś³ÉĒāĘų”¢IĘųĢåŗĶĒāŃõ»ÆÄĘ£¬ĒŅJæÉ×÷ɱ¾śĻū¶¾¼Į£¬ĪŖ“ĪĀČĖįŃĪ£¬ĖłŅŌIŹĒCl2£¬µē½ā±„ŗĶŹ³ŃĪĖ®ÖĘČ”ĀČĘų£¬ĖłŅŌHŹĒNaCl£¬ĒāĘųŗĶĀČĘų·“Ӧɜ³ÉG£¬ĖłŅŌGŹĒHCl£»ĀČĘųŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬ĖłŅŌJŹĒNaClO£¬
£Ø1£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬BŹĒ¹żŃõ»ÆÄĘ£¬¹żŃõ»ÆÄĘĪŖĄė×Ó»ÆŗĻĪļ£¬Ęäµē×ÓŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©DĪŖNaOH”¢EĪŖH2O£¬ĒāŃõ»ÆÄĘÓėĮņĖį·“Ӧɜ³É1molĖ®·Å³öµÄČČĮæĪŖakJ£¬ŌņNaOHÓėH2SO4ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗNaOH£Øaq£©+$\frac{1}{2}$H2SO4£Øaq£©=$\frac{1}{2}$Na2SO4£Øaq£©+H2O£Øl£©”÷H=-akJ/mol£¬
¹Ź“š°øĪŖ£ŗNaOH£Øaq£©+$\frac{1}{2}$H2SO4£Øaq£©=$\frac{1}{2}$Na2SO4£Øaq£©+H2O£Øl£©”÷H=-akJ/mol£»
£Ø3£©·“Ó¦¢ŚĪŖ¹żŃõ»ÆÄĘÓėĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Na2O2+2H2O=4Na++4OH-+O2”ü£»
·“Ó¦¢ŻĪŖµē½ā±„ŗĶŹ³ŃĪĖ®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Cl-+2H2OØTCl2”ü+H2”ü+2OH-£¬
¹Ź“š°øĪŖ£ŗ2Na2O2+2H2O=4Na++4OH-+O2”ü£»2Cl-+2H2OØTCl2”ü+H2”ü+2OH-£»
£Ø4£©HĪŖNaCl£¬µē½āµĪ¼ÓÓŠÉŁĮæ·ÓĢŖµÄHµÄ±„ŗĶČÜŅŗ·¢Éś2NaCl+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2NaOH+Cl2”ü+H2”ü£¬ĒāĄė×ÓŌŚŅõ¼«·ÅµēĶ¬Ź±Éś³ÉĒāŃõøłĄė×Ó£¬ŌņĪŽÉ«±äĪŖŗģÉ«£¬ČōÓĆFĪŖH2”¢CĪŖO2×é³Éµē³Ų£ØČŪČŚK2CO3×öµē½āÖŹ£©¹©µē£¬Ōµē³ŲÖŠøŗ¼«µē¼«·“Ó¦ĪŖ2H2-4e-+2CO32-=2H2O+2CO2£¬Õż¼«µē¼«·“Ó¦ĪŖ£ŗO2+2CO2+4e-=2CO32-£¬
¹Ź“š°øĪŖ£ŗŅõ£»O2+4e-+2CO2=2CO32-£»
£Ø5£©µČĢå»ż»ģŗĻŗóBaCl2ČÜŅŗµÄÅضČĪŖ£ŗ$\frac{1}{2}$”Į4.0”Į10 -6mol/L=2.0”Į10 -6mol/L£¬
ŌņÉś³ÉBaSO4³ĮµķĖłŠčSO42-Ąė×ÓµÄ×īŠ”ÅضČĪŖ£ŗc£ØSO42-£©=$\frac{1.0”Į1{0}^{-10}}{2.0”Į1{0}^{-6}}$mol/L=5.0”Į10-5mol/L£¬»ģŗĻĒ°ĮņĖįČÜŅŗµÄÅضČĪŖ1.0”Į10-4mol/L£¬ŌņĒāĄė×ÓµÄ×īŠ”ÅضČĪŖ2.0”Į10-4mol/L£¬
ĖłŅŌÉś³É³ĮµķĖłŠčH2SO4ČÜŅŗµÄ×ī“ópH=-lg2.0”Į10-4=4-lg2”Ö3.7£¬
¹Ź“š°øĪŖ£ŗ3.7£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬ĢāÄæÄѶČÖŠµČ£¬”°BĪŖµ»ĘÉ«·ŪÄ©£¬EŌŚ³£ĪĀĻĀĪŖŅŗĢå”±ĪŖĶʶĻĶ»ĘĘæŚ£¬×¢ŅāŹģĮ·ÕĘĪÕ³£¼ūŌŖĖŲ¼°Ęä»ÆŗĻĪļŠŌÖŹ£¬ŹŌĢāÖŖŹ¶µć½Ļ¶ą”¢×ŪŗĻŠŌ½ĻĒ棬³ä·Öæ¼²éĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Āß¼ĶĘĄķÄÜĮ¦£®


 A¼Ó½šĢā ĻµĮŠ“š°ø
A¼Ó½šĢā ĻµĮŠ“š°ø Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaCl£ŗĪŅŹĒĄė×Ó»ÆŗĻĪļ£¬ŗ¬ÓŠ¼«ŠŌ¼ü | |
| B£® | H2O£ŗĪŅ1molÖŠŗ¬ÓŠ2mol·Ē¼«ŠŌ¼ü | |
| C£® | KOH£ŗ¼Čŗ¬ÓŠĄė×Ó¼ü£¬ÓÖŗ¬ÓŠ¼«ŠŌ¹²¼Ū¼ü | |
| D£® | NaNO3£ŗĪŅŹĒŗ¬ÓŠĄė×Ó¼üµÄ¹²¼Ū»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×Ķ锢ŅŅĻ© | B£® | ŅŅĶ锢ŅŅĻ© | C£® | ŅŅĶ锢±ūĻ© | D£® | ¼×Ķ锢±ūĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
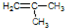 £®
£® £®
£®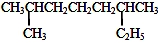 µÄĻµĶ³ĆüĆūŹĒ2£¬6-¶ž¼×»łŠĮĶ飮
µÄĻµĶ³ĆüĆūŹĒ2£¬6-¶ž¼×»łŠĮĶ飮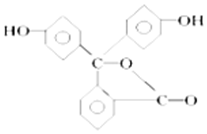
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
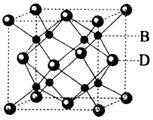 ÓŠA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲ£¬ĘäÖŠAŌŖĖŲµÄŅ»ÖÖŗĖĖŲƻӊ֊×Ó£¬BŌŖĖŲµÄµēøŗŠŌ×ī“ó£¬CŌŖĖŲµÄ»łĢ¬Ō×ÓL²ćÉĻÓŠČżøöĪ“³É¶Ōµē×Ó£¬DŌŖĖŲĪŖÖ÷×åŌŖĖŲĒŅÓėEŌŖĖŲĶ¬ÖÜĘŚ£¬Ęä×īĶāµē×Ó²ćÉĻÖ»ÓŠĮ½øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£¬EŌŖĖŲÓŠĮ½ÖÖ³£¼ūŃõ»ÆĪļE2O”¢EO£¬ĘäÖŠE2OĪŖשŗģÉ«£®Ēė»Ų“š£ŗ
ÓŠA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲ£¬ĘäÖŠAŌŖĖŲµÄŅ»ÖÖŗĖĖŲƻӊ֊×Ó£¬BŌŖĖŲµÄµēøŗŠŌ×ī“ó£¬CŌŖĖŲµÄ»łĢ¬Ō×ÓL²ćÉĻÓŠČżøöĪ“³É¶Ōµē×Ó£¬DŌŖĖŲĪŖÖ÷×åŌŖĖŲĒŅÓėEŌŖĖŲĶ¬ÖÜĘŚ£¬Ęä×īĶāµē×Ó²ćÉĻÖ»ÓŠĮ½øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£¬EŌŖĖŲÓŠĮ½ÖÖ³£¼ūŃõ»ÆĪļE2O”¢EO£¬ĘäÖŠE2OĪŖשŗģÉ«£®Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČÜÖŹ | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
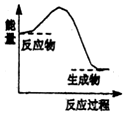
| A£® | ĒāŃõ»Æ¼ŲÓėĮņĖįµÄ·“Ó¦ | |
| B£® | ½šŹōĆ¾ÓėŃĪĖįµÄ·“Ó¦ | |
| C£® | øßĪĀĢõ¼žĻĀĢ¼·ŪÓė¶žŃõ»ÆĢ¼µÄ·“Ó¦ | |
| D£® | Ba£ØOH£©2•8H2O¾§ĢåÓėNH4Cl¹ĢĢåµÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
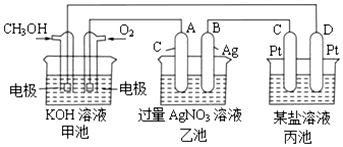
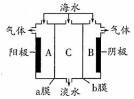 ŗ£Ė®ÖŠŗ¬ÓŠ“óĮæNa+”¢C1-¼°ÉŁĮæCa2+”¢Mg2+”¢SO42-£¬ÓƵēÉųĪö·Ø¶ŌøĆŗ£Ė®ŃłĘ·½ųŠŠµ»Æ“¦Ąķ£¬ČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŗ£Ė®ÖŠŗ¬ÓŠ“óĮæNa+”¢C1-¼°ÉŁĮæCa2+”¢Mg2+”¢SO42-£¬ÓƵēÉųĪö·Ø¶ŌøĆŗ£Ė®ŃłĘ·½ųŠŠµ»Æ“¦Ąķ£¬ČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | bĤŹĒŃōĄė×Ó½»»»Ä¤ | |
| B£® | A¼«ŹŅ²śÉśĘųÅŻ²¢°éÓŠÉŁĮæ³ĮµķÉś³É | |
| C£® | µ»Æ¹¤×÷Ķź³ÉŗóA”¢B”¢CČżŹŅÖŠpH“óŠ”ĪŖpHA£¼pHB£¼pHC | |
| D£® | B¼«ŹŅ²śÉśµÄĘųĢåæÉŹ¹ŹŖČóµÄKIµķ·ŪŹŌÖ½±äĄ¶ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com