
| A. | 火山爆发产生的气体 | B. | 大气中二氧化碳含量增加 | ||
| C. | 乱砍乱伐森林,破坏了生态环境 | D. | 工业上大量燃烧含硫燃料 |
分析 酸雨的形成是一种复杂的大气化学和大气物理过程,一般认为,酸雨是由于排放的SO2和氮氧化物等酸性气体进入大气后,造成局部地区中的SO2富集,在水凝过程中溶解于水形成亚硫酸[SO2+H2O=H2SO3],然后经某些污染物的催化作用及氧化剂的氧化作用生成硫酸[2H2SO3+O2=2H2SO4],随雨水降下形成酸雨,以此解答该题.
解答 解:A.火山爆发产生的气体含有二氧化硫,可产生酸雨,但不是主要原因,故A不选;
B.二氧化碳可导致温室效应,但不导致酸雨,故B不选;
C.乱砍乱伐森林,破坏了生态环境,不会改变空气中二氧化硫、氮氧化物的含量,不会导致酸雨,故C不选;
D.工业上大量燃烧含硫燃料和以含硫矿石为原料的金属冶炼,产生的二氧化硫气体排放到大气中是形成酸雨的主要原因,故D选.
故选D.
点评 本题考查三废处理及环境保护,为高频考点,把握物质的性质、环境保护、酸雨的形成为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:选择题
| A. | D216O、HTl6O共10g,所含分子数为0.25NA | |
| B. | 25g质量分数68%的H2O2水溶液中含氧原子数目为NA | |
| C. | 常温下1L0.1 mol/L A1C13溶液中阳离子数大于0.1NA | |
| D. | 1L0.1 mol/L Fe(NO3)3溶液参加反应,最多转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
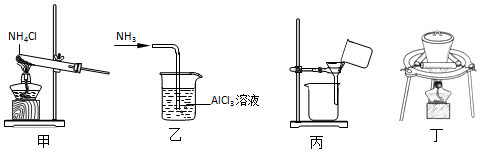
| A. | 用装置甲制取NH3 | B. | 用装置乙制备Al(OH)3 | ||
| C. | 用装置丙进行过滤操作 | D. | 用装置丁灼烧Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
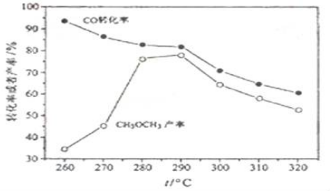 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源,由合成气(组成为H2、CO、少量CO2)直接制备二甲醚,其中主要过程包括以下四个反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源,由合成气(组成为H2、CO、少量CO2)直接制备二甲醚,其中主要过程包括以下四个反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 难容电解质 | AgCl | AgBr | Agl | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10 -17 | 1.4×10-5 | 1.12×10-12 |
| A. | 由溶度积常数可以判断相应物质的溶解性大小 | |
| B. | 将等体积的 4×10-3 mol/L 的 AgNO3 溶液和 4×10-3 mol/L K2CrO4溶液混合,有 Ag2CrO4沉淀产生 | |
| C. | 向 AgCl 的悬浊液中滴加饱和 NaBr 溶液不能得到黄色 AgBr | |
| D. | 向 100 mL 0.02mol/L 的 NaSO4 溶液中加入 100mL0.02mol/L 的 AgNO3 溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
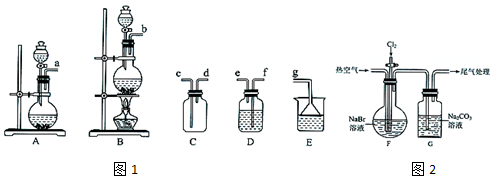
| 操作步骤 | 实验现象 | 结论或解释 |
| ①去适量G中溶液于试管中,加入硫酸酸化 | 产生气泡 | G中溶液含有CO32-或HCO3- |
| 向①的试管中加入CCl4,振荡,静置 | ②溶液分层,下层为棕红色 | 生成单质溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 因患“禽流感”而被捕杀的家禽尸体常用生石灰处理 | |
| C. | 《本草经集注》中记载了区分硝石(KNO3)和朴消(Na2SO4)的方法:“以火烧之,紫青烟起,乃真硝石也”;这是利用了“焰色反应” | |
| D. | 煤经过气化和液化等物理变化可以转化为清洁燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com