
| 11.2g |
| 56g/mol |
| 11.2g |
| 56g/mol |
| 0.4mol |
| 0.2L |
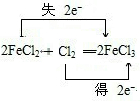 ,
, .
.


科目:高中化学 来源: 题型:
| A、51 | B、94 |
| C、141 | D、145 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验乙醛中的醛基:在一定量CuSO4溶液中,加入少量NaOH溶液,然后再加入乙醛,加热产生砖红色沉淀 |
| B、分离提纯苯:向苯和苯酚混合溶液中加入足量浓溴水,静置后分液 |
| C、比较CH3COO-和CO32-结合H+的能力:相同温度下,测定浓度均为0.1mol?L-1的Na2CO3和CH3COONa溶液的pH |
| D、检验溴乙烷中的溴元素:向某溴乙烷中加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
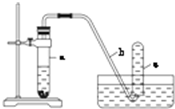 用如图所示的装置进行实验:
用如图所示的装置进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度为
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度为查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,在容积为1L的密闭容器中发生可逆反应:Fe(s)+H2O(g)═FeO(s)+H2(g)△H>0.在1000℃时,H2O(g)的平衡转化率(α)与体系总压强(p)关系如图所示.
一定条件下,在容积为1L的密闭容器中发生可逆反应:Fe(s)+H2O(g)═FeO(s)+H2(g)△H>0.在1000℃时,H2O(g)的平衡转化率(α)与体系总压强(p)关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 取 A、B 两份物质的量浓度相等的 NaOH 溶液,体积均为 50mL,分别向其中通入一定量的 CO2后,再分别稀释为 100mL.
取 A、B 两份物质的量浓度相等的 NaOH 溶液,体积均为 50mL,分别向其中通入一定量的 CO2后,再分别稀释为 100mL.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com