
下列说法不正确的是
A.化学反应过程中既有物质变化又有能量变化,能量的释放或吸收以物质变化为基础
B.研究化学反应进行的方向、快慢和限度是化学反应原理的重要内容
C.电解质在水溶液中的反应反应速率很高,是因为这类反应不需要活化能来引发
D.大力发展火电以满足工业发展对电力的需求,符合节能减排的要求
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届湖南省长沙市高三上学期第三次月考化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的作用。下列有关说法正确的是
A.福尔马林可作食品的保鲜剂
B.氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应
C.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油
D.浓硫酸可刻蚀石英制艺术品
查看答案和解析>>
科目:高中化学 来源:2016届吉林省扶余市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是
A.Cu(OH)2+HCl;Cu(OH)2+CH3COOH
B.NaHCO3+H2SO4;KHCO3+HCl
C.NaHCO3+NaOH;Ca(HCO3)2+NaOH
D.BaCl2 + H2SO4;Ba(OH)2+H2SO4
查看答案和解析>>
科目:高中化学 来源:2016届山东省淄博市高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.1mol.L-1的Ca(ClO)2溶液中含Ca2+数目为NA
B.22.4LCl2分别与足量的Cu、Fe完全反应转移电子数分别为2NA、3NA
C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.1 mol -OH与1 molOH-所含电子数均为9 NA
查看答案和解析>>
科目:高中化学 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:选择题
化学知识在生产和生活中有着重要的应用。下列说法中正确的是
① 钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等
② K、Na合金可作原子反应堆的导热剂
③ 明矾常作为消毒剂
④ Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等
⑤ 碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥ 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
A.①②③④ B.①②④⑥ C.①②③④⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期开学联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.需要加热的化学反应都是吸热反应
B.陶瓷、玻璃和水泥都是无机非金属材料
C.醋酸、蔗糖均属于电解质
D.糖类、油脂和蛋白质都能发生水解反应
查看答案和解析>>
科目:高中化学 来源:2016届广西省高三上学期第一次月考理综化学试卷(解析版) 题型:填空题
【化学选修——2:化学与技术】
水处理技术在生产、生活中应用广泛。
(1)根据水中Ca2+、Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。
①硬水软化的方法通常有___________、__________和离子交换法。离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树脂置于______________中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,__________洗涤效果较好,原因是__________________。
(2)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾。请解释这一做法的原因:__________。(用必要的离子方程式和文字描述)。
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是___________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省西安市高一上10月月考化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.在标准状况下,1mol任何物质的体积为22.4L
B.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等
C.1molH2和1molHe中,所含的分子数相同,原子数相同,质量也相同
D.体积为6L的O2,其质量可能为8g
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期期中考试理综化学试卷(解析版) 题型:填空题
(15分)冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①在一定条件下,在一个容积固定为2L的密闭容器中充入0.8molNO和1.20molCO,开始反应至3min时测得CO的转化率为20%,则用N2表示的平均反应速率为V(N2)=____________________。
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=________________。
③该反应在低温下能自发进行,该反应的△H_________0,(选填“>”、“=”或“<”)
④在某一绝热,恒容的密闭容器中充入一定量的NO、CO发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知t2—t1=t3—t2)。
则下列说法不正确的是__________。(填编号)
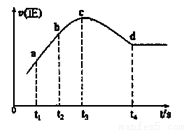
A.反应在c点未达到平衡状态
B.反应速率a点小于b点
C.反应物浓度a点大于b点
D.NO的转化率t1—t2=t2—t3
(2)使用甲醇汽油可能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通人3mol CO,此时v(正)__________ v(逆)(选填‘‘>”、“<’’或“=”),判断的理由__________________。
(3)二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为:
2CO(g)+4H2(g)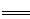 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
已知一定条件下,该反应中CO的平衡转化率随温度、投料比 的变化曲线如图:
的变化曲线如图:
①a、b、c按从大到小的顺序排序为___________。
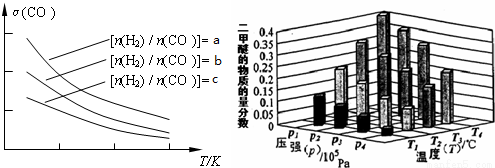
②某温度下,将2.0mol CO(g)和4.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如上图所示,关于温度和压强的关系判断正确的是___________;
A.P3>P2,T3>T2 B.P1>P3,T1>T3 C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是___________:
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积百分含量增大
E.混合气体的密度减小
F.氢气的转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com