
【题目】海水占地球总蓄水量的97.2%,若把海水的淡化和化工生产结合起来,就可充分利用海洋资源来解决淡水资源缺乏的问题。
(1)氯化钠中的金属元素在周期表中的位置是_________;
(2)目前常用的“海水淡化”主要技术之一是蒸馏法,蒸馏法属于________(填“物理变化”或“化学变化”)。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据要求回答问题:
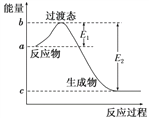
(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。
(2)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
(3)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为____________________________________________________________________。
(4)在微生物作用的条件下,NH经过两步反应被氧化成NO。这两步的能量变化如图:
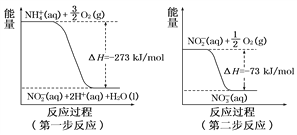
第二步反应是__________反应(填“放热”或“吸热”)。1 mol NH(aq)全部氧化成NO(aq)的热化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁红涂料中添加有CuO或FeO中的一种,为探究添加物的成分设计如下实验方案。
(1)请写出实验步骤、预期现象,对应的离子方程式。
(限选试剂:铁粉、3mol/LH2SO4、0.1mol/L酸性KMnO4溶液、10%H2O2、KSCN溶液)

①_____________,②_____________,_____________,③___________,_____________
④操作步骤③中反应的离子方程式为____________。
(2)经分析该铁红涂料中有FeO,为测定铁红中铁的质量分数,兴趣小组的同学称量11.6g该铁红涂料进行了如下实验。
已知:气体由草酸晶体受热分解得到:H2C2O4·2H2O ![]() CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。
CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。

①装置A、B中的试剂依次是_____、______。
②气体通入后,接下来的操作是____,然后对C装置加热。
③实验前后称得D装置增重8.8g,则此铁红中铁的质量分数是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
A. 可用电解熔融CeO2制取金属铈,铈在阳极生成
B. ![]() 、
、![]() 是同素异形体
是同素异形体
C. 铈的原子核外有58个电子
D. 铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素是第一个人工合成的有机物。下列关于尿素的叙述中不正确的是( )
A.尿素是一种氮肥
B.尿素是人体新陈代谢的一种产物
C.尿素能发生水解反应
D.尿素是一种酸性物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】28g铜、银合金与一定量某浓度的硝酸溶液反应,金属完全溶解,放出的气体与2.24L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中铜的质量是( )
A.3.2g
B.6.4g
C.12.8g
D.21.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com