
| A、Na和O2 |
| B、NaOH和CO2 |
| C、Na2CO3和HCl |
| D、NaHCO3和NaOH |


科目:高中化学 来源: 题型:
| A、加入少量的CH3COONa固体 |
| B、加入少量NaOH固体 |
| C、加入少量NaHCO3固体 |
| D、通入少量HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测定同浓度的盐酸、硼酸溶液的导电能力 |
| B、常温下,用pH计测定硼酸钠溶液的pH |
| C、将碳酸钠溶液滴入硼酸溶液中,无明显现象 |
| D、将硼酸溶液稀释2倍后,用pH试纸测定其pH变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、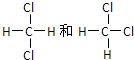 |
B、CH2═CH-CH═CH2和 |
| C、CH3C(CH3)2C(CH3)3 和CH3(CH2)3C(CH3)3 |
D、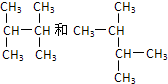 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO |
| B、CO2 |
| C、CO和 CO2 |
| D、C2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释溶液,水解平衡常数增大 | ||
| B、通入H2S,HS-浓度增大 | ||
C、升高温度,
| ||
| D、加入NaOH固体,溶液pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
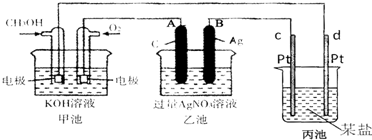
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、土壤中离子的吸附和交换过程,有保肥作用 |
| B、将植物油倒入水中用力搅拌形成油水混合物 |
| C、一束平行光线射入蛋白质溶液里,可以看到一条光亮的通路 |
| D、氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 过氧乙酸 本品包括甲、乙两种溶液,体积各500mL,把甲、乙溶液各1份在玻璃容器中混合后放置24小时后,其中过氧乙酸浓度不少于10%,应用50倍纯水稀释(浓度为0.2%)稀释后才能使用. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com