
| A. | 新制氯水只含Cl2和H2O两种分子 | B. | 氢氟酸不能贮放在玻璃瓶里 | ||
| C. | 光导纤维的主要成分是二氧化硅 | D. | 浓硫酸用铁制容器密封保存 |
分析 A.氯气通入水中反应生成次氯酸和盐酸;
B.氢氟酸能与玻璃反应生成四氟化硅气体;
C.二氧化硅为光导纤维的主要成分;
D.浓硫酸在常温下能够与铁发生钝化现象,阻止了反应的继续进行.
解答 解:A.氯气通入水中反应生成次氯酸和盐酸,还有次氯酸分子,故A错误;
B.氢氟酸能与玻璃反应生成四氟化硅气体,应保存在塑料瓶中,故B正确;
C.光导纤维中所用材料为二氧化硅,故C正确;
D.在常温下浓硫酸能够与铁发生钝化,所以浓硫酸可以用铁制容器密封保存,故D正确.
故选A.
点评 本题考查了常见化学试剂的保存方法判断,题目难度不大,注意掌握常见化学试剂的性质及正确的保存方法,明确见光分解的物质需要不存在棕色试剂瓶中、能够与二氧化硅反应的试剂不能用玻璃塞的试剂瓶、氢氟酸不能使用玻璃瓶保存等.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:解答题
 (增塑剂)②
(增塑剂)② (合成橡胶原料)③CH3CH2CH2CH2OH(萃取剂)
(合成橡胶原料)③CH3CH2CH2CH2OH(萃取剂) 香料)
香料)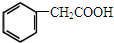 (植物生长刺激素)
(植物生长刺激素)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na十2H2O═=2NaOH十H2↑ | B. | 2H2O═2H2↑十O2↑ | ||
| C. | 2F2十2H2O═4HF十O2 | D. | SO3十H2O═H2S04 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol NaOD溶于重水制成1L溶液,pD=11 | |
| B. | 将pD为4的DCl的重水溶液稀释10倍,所得溶液pD为5 | |
| C. | 向30 mL 0.5mol•L-1NaOD的重水溶液中加入20 mL 0.5 mol•L-1DCl的重水溶液,所得溶液pD=10 | |
| D. | pD=10的NaOD的重水溶液中,由重水电离出的c(OD-)为1×10-10mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com