
| ||
| ||
| ||
| ||


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源:2011-2012学年北京市朝阳区高一下学期期末统一考试化学试卷(带解析) 题型:填空题
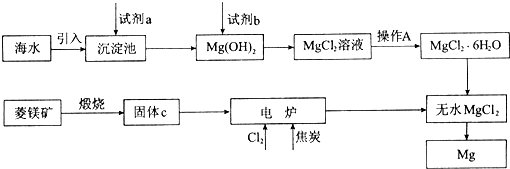
(7分)金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
查看答案和解析>>
科目:高中化学 来源:2014届北京市朝阳区高一下学期期末统一考试化学试卷(解析版) 题型:填空题
(7分)金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:

回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
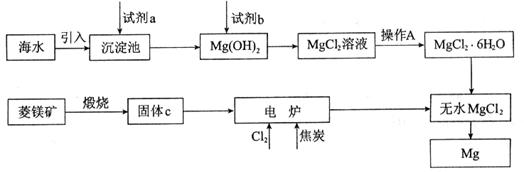
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市朝阳区高一(下)期末化学试卷(解析版) 题型:解答题
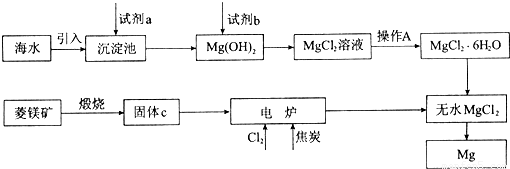
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com