
| A. | SO2>I->Fe2+>Cl- | B. | Cl->Fe2+>SO2>I- | C. | Fe2+>I->Cl->SO2 | D. | I->Fe2+>Cl->SO2 |
分析 依据氧化还原反应的强弱规律,根据元素的化合价升高来判断还原剂,利用氧化还原反应中还原剂的还原性大于还原产物的还原性来解答.
解答 解:①I2+SO2+2H2O═H2SO4+2HI中,S元素的化合价升高,I化合价降低,由还原剂的还原性大于还原产物的还原性,则还原性SO2>I-,
②2FeCl3+2HI═2FeCl2+I2+2HCl中,I元素的化合价升高,Fe化合价降低,由还原剂的还原性大于还原产物的还原性,则还原性I->Fe2+,
③2FeCl2+Cl2═2FeCl3中,Fe元素的化合价升高,Cl化合价降低,由还原剂的还原性大于还原产物的还原性,则还原性Fe2+>Cl-,
所以离子的还原性由强到弱的顺序为SO2>I->Fe2+>Cl-,
故选A.
点评 本题考查了氧化性强弱的比较,难度不大,根据“同一化学反应中,氧化剂的还原性大于还原产物的还原性”来分析解答即可.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:选择题
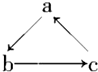 Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )| 选项 | A | B | C | D |
| a | Na | Al | Fe | Cu |
| b | NaOH | Al2O3 | FeCl3 | CuSO4 |
| c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl=H+1+Cl-1 | B. | (NH4)2SO4=(NH4)2-+SO42- | ||
| C. | FeCl2=Fe3++Cl- | D. | K2S=2 K++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应一定伴随有热量的变化 | |
| B. | 活化能越大的化学反应其反应热数值也越大 | |
| C. | 反应热的产生是由于生成物与反应物的总能量不同 | |
| D. | 放热反应是由于反应物键能总和大于生成物键能总和 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽马鞍山二中高一10月阶段测化学卷(解析版) 题型:选择题
在同温、同压下,A容器的氮气和B容器的氨气中,若它们所含的原子数相等,则这两个容器的体积之比是
A.2:1 C.2:3 B.1:2 D.1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com