(1)0.5mol H2O的质量为______,其中共含有______个原子.
(2)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是______(填分子式,下同),在相同温度和相同压强条件下,体积最大的是______.
(3)在______mL 0.2mol/L NaOH溶液中含1g溶质;配制50mL 0.2mol/L CuSO4溶液,需要CuSO4?5H2O______g.
解:(1)m(H
2O)=0.5mol×18g/mol=9g,共含有原子数为:N=3×0.5×N
A=9.01×10
23,故答案为:9g;9.01×10
23;
(2)已知:M(HCl)=36.5g/mol,M(NH
3)=17g/mol,M(CO
2)=44g/mol,M(O
2)=32g/mol,
由n=

=

=
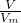
可知,相同质量时,摩尔质量越大,气体的物质的量越小,体积越小,则
含有分子数目最少的是CO
2,在相同温度和相同压强条件下,体积最大的是NH
3,
故答案为:CO
2;NH
3;
(3)n(NaOH)=
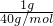
=0.025mol,
V×0.2mol/L=0.025mol,
V=0.125L,即125ml,
n( CuSO
4)=0.05L×0.2mol/L=0.01mol,
m(CuSO
4?5H
2O )=0.01mol×250g/mol=2.5g,
故答案为:125;2.5.
分析:(1)根据n=

=

结合分子的组成计算;
(2)根据n=

=

=
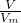
计算;
(3)根据n=

=cV计算.
点评:本题考查物质的量的相关计算,题目难度不大,注意相关计算公式的运用.

 =
= =
=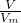 可知,相同质量时,摩尔质量越大,气体的物质的量越小,体积越小,则
可知,相同质量时,摩尔质量越大,气体的物质的量越小,体积越小,则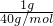 =0.025mol,
=0.025mol, =
= 结合分子的组成计算;
结合分子的组成计算; =
= =
=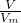 计算;
计算; =cV计算.
=cV计算.

 阅读快车系列答案
阅读快车系列答案