
某盐桥式电池如图所示.下列说法不正确的是( )
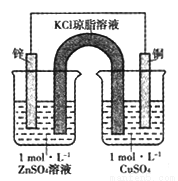
A. 电子由锌电极流向铜电极
B. 将锌、铜电极互换也能形成原电池
C. U型管中的K+向铜电极移动
D. 铜电极反应式是Cu2++2e-=Cu
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
如图,A、B、C、D、E是元素周期表中的5种主族元素。下列说法不正确的是( )

A. A、E原子序数之差可能为2
B. D、E原子序数之差可能是8、18或32
C. B、C原子序数之差一定是2
D. B、D原子序数之差不可能是7
查看答案和解析>>
科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:填空题
SO2是常见的大气污染物,燃煤是产生SO2的主要原因。工业上有多种方法可以减少SO2的排放。
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的化学方程式是 。
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
① 分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO3时,两种吸收液体积比V(Na2SO3):V(NaOH)= 。
② NaOH溶液吸收了足量的SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是 。
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气密性已检验):


已知:Na2SO3(固体) + H2SO4(浓)  Na2SO4 + SO2↑+ H2O
Na2SO4 + SO2↑+ H2O
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3,所以BaCl2溶液可做SO2吸收液。
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是:
① A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀。
② 。
为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现象;D中红色褪去。
③试管B中试剂是 溶液;滴加浓硫酸之前的操作是 。
④通过甲乙两位同学的实验,得出的结论是 。
查看答案和解析>>
科目:高中化学 来源:安徽省皖北协作区2017届高三第19届(3月)联考理综化学试卷 题型:选择题
一种三室微生物电池污水系统原理如下图所示,图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是

A. 该装置为原电池,b是原电池的负扱
B. 中间室:Na+移向右室,Cl-移向左室,a极区溶液的pH滅小
C. b极反应式为2NO3- -10e-+12H+=N2↑+6H2O
D. 当左室有4.48LCO2(标准状况下)生成时,右室产生N2的物质的量为0.8mol
查看答案和解析>>
科目:高中化学 来源:2017届高考信息卷(全国卷I)理科综合(一)化学试卷(解析版) 题型:填空题
铁及其化合物在日常生活中有广泛的应用,回答下列问题。
(1)FeC13具有净水作用,但腐蚀设备,FeC13溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________。
(2)为节约成本,工业上用NaC1O、氧化酸性FeCl2废液得到FeC13,完成NaClO3氧化FeCl2的离子方程式:___________。
口ClO3-+口Fe2++口_____=口Cl-+口Fe3++口_______。
(3)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景。其生产工艺如图1所示:
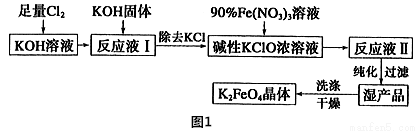
①实验室模拟工业流程中过滤操作用到的主要玻璃仪器有______。
②在“反应液I”中加KOH固体的目的有两个,a是与“反应液I”中过量的Cl2继续反应,生成更多的KClO, b是_____。
③用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是______(用离子方程式表示)。
(4)从环境保护的角度看,制备K2FeO4较好的方法未电解法,其装置如图2所示。
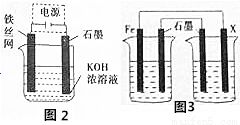
电解过程中阳极电极反应式为________。
(5)钢铁腐蚀造成很大损失,有资料显示,全世界每年由于腐蚀二造成的报废的钢铁高达总产量的三分之一。防止钢铁腐蚀有很多措施,用图3装置防止钢铁腐蚀(烧杯中均为食盐水), X 极的电极材料应是______(填字母)。
A.锌 B.铜 C.银 D.石墨
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:计算题
有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀;滤液与4.0mol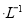 NaOH溶液反应,用去35mL碱液时恰好完全中和。试求:
NaOH溶液反应,用去35mL碱液时恰好完全中和。试求:
(1)混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取l0mL原混合液,加入3.2g铜粉共热时,在标准状况下收集到气体的体积为多少升?(保留两位有效数字。)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:选择题
下列每组物 质中含有的化学键类型相同的是( )
质中含有的化学键类型相同的是( )
A.NaCl、HCl、H2O、NaOH B.Cl2、Na2S、HCl、SO2
C.HBr、CO2 、H2O、CS2 D.Na2O2、H2O2、H2O、O3
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(三)化学试卷(解析版) 题型:实验题
从某废触媒[主要成分为活性炭、ZnO、FeO、(CH3COO)2Zn]中制取醋酸锌晶体的实验步骤如下:

(1)浸取时,在三口烧瓶中加入废触媒及稀醋酸,给三口烧瓶加热并同时开动搅拌器的目的是___________。
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是____________。抽滤时用的硅酸盐质仪器有________和________。
(3)流程图中加入H2O2的目的是_______________。
(4)所得晶体(CH3COO)2Zn·2H2O热重分析(TG/%=固体样品的剩余质量/固体样品的起始质量),文献表明分解分三个阶段,在200°C以下脱去两分子结晶水,形成的(CH3COO)2Zn在242°C熔融,370°C完全分解为ZnO同时生成CO2及一种含氧衍生物(核磁共振氢谱只有1组峰)。(CH3COO)2Zn分解生成氧化锌的反应方程式为_____________。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二3月月考化学试卷(解析版) 题型:选择题
香草醛用作化妆品的香精和定香剂,也是食品香料和调味剂,还可做抗癫痫药。香草醛的分子结构如图,下列关于香草醛的说法中,不正确的是( )
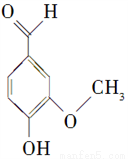
A. 该化合物的分子式为C8H6O3
B. 遇FeCl3溶液会显紫色
C. 最多能与4 mol H2发生加成反应
D. 与香草醛有相同官能团且苯环上有三个取代基的香草醛的同分异构体(包括香草醛)有10种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com