
| A、①④⑤ | B、③⑤ | C、④⑤ | D、全部 |


科目:高中化学 来源: 题型:
 某学习小组利用中和反应原理测定某氨水的物质的量浓度,以测量溶液导电性判断滴定终点.实验步骤如下:
某学习小组利用中和反应原理测定某氨水的物质的量浓度,以测量溶液导电性判断滴定终点.实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类和蛋白质都能发生水解反应 |
| B、鸡蛋清和淀粉溶液可以用浓硝酸鉴别 |
| C、甲苯和乙酸在一定条件下都能发生取代反应 |
| D、植物油和石油的裂化产物均能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3 |
| B、CaSO3 |
| C、NaOH |
| D、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池.其工作原理如图所示.下列有关说法正确的是( )
生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池.其工作原理如图所示.下列有关说法正确的是( )| A、、O2在C2电极上得电子,被氧化 |
| B、电子由C2极经外电路流向C1极 |
| C、每转移6mole-1,理论上生成22.4LCO2 |
| D、C1极的电极反应式为:C2H5OH+3H2O-12e-1=2CO2+12H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
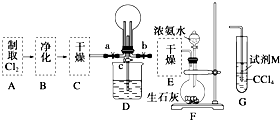 某化学兴趣小组的同学进行Cl2、NH3的制备及性质检验等实验的流程和部分装置如图:
某化学兴趣小组的同学进行Cl2、NH3的制备及性质检验等实验的流程和部分装置如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com