
【题目】由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的pH值
A. 不变 B. 先变小后变大 C. 逐渐变大 D. 逐渐变小
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质的区分方法不正确的是
A. 用碘酒区分淀粉溶液与蛋白质溶液
B. 用AgNO3溶液区分NaCl与KCl溶液
C. 用澄清石灰水区分CO与CO2气体
D. 用石蕊试液区分稀H2SO4与NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列有关晶体的叙述中错误的是 ( )
A. 离子晶体中,一定存在离子键B. 原子晶体中,只存在共价键
C. 金属晶体的熔沸点均很高D. 稀有气体的原子能形成分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中
(1)该反应的氧化剂是 , 氧化产物是
(2)该反应的离子方程式为
(3)请用“双线桥法”标出该反应电子转移的方向和数目.
(4)该反应氧化剂与还原剂的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O
试通过计算和推理完成下面的问题:
(1)SO2物质可以使酸性KMnO4溶液褪色,此反应中(填写化学式)失去电子.
(2)足量的铜片与 含溶质1.8mol的浓H2SO4充分反应,如果该反应过程中转移了 0.2mol电子,生成的CuSO4的质量为克,生成的气体在标准状况下体积为升(假设气体全部逸出).
(3)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应.请写出此过程发生的反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关环境问题的说法正确的是( )
A.燃煤时加入适量石灰石,可减少废气中CO的量
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.严格执行机动车尾气排放标准有利于防止大气污染
D.pH在5.6~7.0之间的降水通常称为酸雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷是生物体中不可缺少的元素之一,它能形成多种化合物. 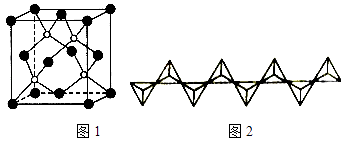
(1)基态磷原子中,电子占据的最高能层符号为;该能层中电子占据的能量最高的电子云在空间有个伸展方向,原子轨道呈形.
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为 .
(3)单质磷与Cl2反应,可以生成PCl3和PCl5 . 其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为 , 其分子的空间构型为 .
(4)磷化硼(BP)是一种超硬耐磨涂层材料,如图1为其晶胞,硼原子与磷原子最近的距离为acm.用Mg/mol表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为 .
(5)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+ . 基态Fe3+的核外电子排布式为;PO43﹣作为为Fe提供 .
(6)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类.某直链多磷酸钠的阴离子呈如图2所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连.则该多磷酸钠的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH﹣ ![]() 2CO32﹣+6H2O,则下列说法正确的是( )
2CO32﹣+6H2O,则下列说法正确的是( )
A.构成该电池的正极和负极必须是两种活性不同的金属
B.充电时有CH3OH生成的电极为阳极
C.放电时电解质溶液的pH逐渐增大
D.放电时负极的电极反应为:CH3OH﹣6e﹣+8OH﹣═CO32﹣+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com