
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
⑴兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。

①通入Cl2后,观察到的现象是 根据现象可得出的结论是___ __。
②集气瓶B发生反应的离子方程式是______ 。
③C装置的作用是______ ,若有2.24 L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子数为________mol。
⑵兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
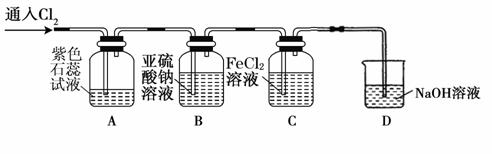
①实验开始后,观察装置A中的现象是: 。
②停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生反应的离子方程式是 。
科目:高中化学 来源: 题型:
某溶液中含有Cl-、SO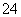 、CO
、CO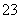 三种离子,每加入一种试剂(分别含Ag+、Ba2+、H+)只除去一种离子,则正确的操作顺序是( )
三种离子,每加入一种试剂(分别含Ag+、Ba2+、H+)只除去一种离子,则正确的操作顺序是( )
A.Ag+、Ba2+、H+
B.Ba2+、H+、Ag+
C.Ba2+、Ag+、H+
D.H+、Ba2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L 1mol/L的FeCl3溶液与0.2L 1 mol/L的KCl溶液中,Cl-的物质的量浓度之比为( )
A.15∶2 B.1∶1 C.3∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质间的每步转化都能通过一步反应实现的是
①Fe→Fe2O3→Fe(OH)3 ② Na→Na2O2→Na2CO3
③ S→SO3→H2SO4→MgSO4 ④ C→CO→CO2→Na2CO3
A.①② B.③④ C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上可用硫酸铝与硫黄焙烧制备氧化铝:2Al2(SO4)3+3S  2Al2O3+9SO2↑,下列有关说法中正确的是( )
2Al2O3+9SO2↑,下列有关说法中正确的是( )
A.反应中Al2(SO4)3被氧化
B.Al2O3是氧化产物
C.该反应中,每转移0.3 mol电子生成5.04 L SO2
D.氧化产物与还原产物的质量之比为1︰2
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,Fe2O3等)提取Al2O3作冶炼铝的原料,由熔盐电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下图所示:
(已知:NaCl熔点为801℃;AlCl3在181℃升华)
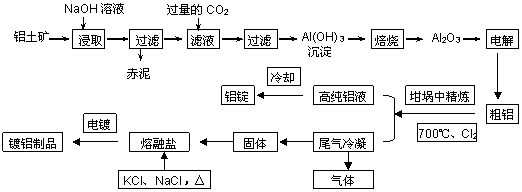
(1)赤泥中的主要成分是 (化学式);向滤液中通入过量CO2所发生反应的离子方程式为 。
(2)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,则铝和氧化铁反应的化学方程式为 。
(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。气泡的主要成分除Cl2外还含有______。固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在________。
(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极的电极反应式为_____________。
(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
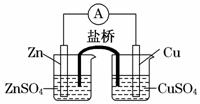
关于如图所示的原电池,下列说法正确的是
A.电子从铜电极通过检流计流向锌电极
B.盐桥中的阳离子向硫酸铜溶液中迁移
C.锌电极发生还原反应,铜电极发生氧化反应
D.铜电极上发生的电极反应是2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知 ( )
A.a的浓度必小于乙酸的浓度
B.a的浓度必大于乙酸的浓度
C.b的浓度必小于乙酸的浓度
D.b的浓度必大于乙酸的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com