
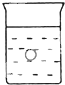
 在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中
在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中

科目:高中化学 来源: 题型:
| A、Fe与FeCl3溶液 |
| B、Na2CO3溶液与HCl |
| C、NaOH溶液与CO2 |
| D、NaOH溶液与AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向溴水中加入NaOH溶液:Br2+2 OH-=BrO-+Br- |
| B、少量H2SO4滴入Ba(OH)2溶液中:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、过量NaHCO3溶液滴入NaHSO4溶液中:HCO3-+H+=H2O+CO2↑ |
| D、在漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤①② | B、③② |
| C、②③④⑤ | D、③④①② |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| SCT陶瓷 |
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.3% |
| B、1.3×10-3% |
| C、0.013% |
| D、1.3×10-3% |
| E、1.3×10-2% |
查看答案和解析>>
科目:高中化学 来源: 题型:


 ,请写出下列反应产物的结构简式:
,请写出下列反应产物的结构简式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com