
【题目】下列所配溶液浓度为1mol/L的是( )
A. 将31g Na2O溶于1L水中 B. 常温下,将22.4LHCl溶于水中,配成1L溶液
C. 将100mL5mol/L的KNO3溶液加水称释至500mL D. 将10mL10mol/L的H2SO4溶液与90mL水混合
【答案】C
【解析】
A、Na2O溶于水,与水反应生成NaOH,为NaOH溶液,根据Na2O质量计算NaOH的物质的量,再根据物质的量浓度定义计算判断,注意水的体积不等于溶液的体积;B、没有标明气体存在的状态是否是标准状况下;C、根据稀释前后溶质的质物质的量不变,即c(浓)V(浓)=c(稀)V(稀);D、根据溶液的体积不具有加和性。
A、根据钠原子守恒可知n(NaOH)=2n(Na2O)=![]() =1mol,但水的体积不等于溶液的体积,所以无法计算,选项A错误;B、没有标明气体存在的状态是否是标准状况下,无法确定气体的物质的量,所以无法计算,选项B错误;C、稀释前后溶质的质物质的量不变,即c(浓)V(浓)=c(稀)V(稀),则0.1L×5mol/L=c(稀)×0.5L,解得c(稀)=1mol/L,选项C正确;D、将10mL10mol/L的H2SO4溶液与90mL水混合溶液的体积要小于100mL,无法计算,选项D错误。答案选C。
=1mol,但水的体积不等于溶液的体积,所以无法计算,选项A错误;B、没有标明气体存在的状态是否是标准状况下,无法确定气体的物质的量,所以无法计算,选项B错误;C、稀释前后溶质的质物质的量不变,即c(浓)V(浓)=c(稀)V(稀),则0.1L×5mol/L=c(稀)×0.5L,解得c(稀)=1mol/L,选项C正确;D、将10mL10mol/L的H2SO4溶液与90mL水混合溶液的体积要小于100mL,无法计算,选项D错误。答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.元素从化合态变为游离态时,该元素一定被还原
B.氧化还原反应的实质是电子的得失或偏移
C.氧化还原反应中一种元素化合价升高一定有另一种元素化合价降低
D.有单质参加或有单质生成的反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ag+与Cl-反应生成氯化银,每次新生成的氯化银有10%见光分解成单质银和氯气,氯气又可以在水溶液中生成HClO3和HCl,而形成的Cl-与剩余的Ag+作用又生成氯化银,这样循环往复直到最终.
(1)依次写出上述各步反应的化学方程式(是离子反应的写离子方程式)____________________ 。
(2)现有1.1molNaCl的溶液,加入足量的硝酸银溶液,问最终能生成___克难溶物(银和氯化银)
(3)最后溶液体积为lL,则H+的物质的量浓度为___ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
A. 该溶液的pH=4
B. 升高温度,溶液的pH增大
C. 此酸的电离平衡常数约为1×10-7
D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )
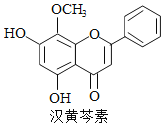
A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液不显色
C. 1 mol该物质与溴水反应,最多消耗2 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化:
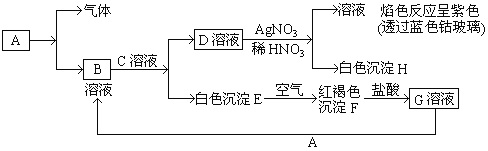
试回答
(1)写出C的化学式____________;
(2)A与水蒸气反应方程式为:__________________________ ;
(3)写出由E转变成F的化学方程式_______________________;
(4)鉴别G溶液中阳离子的方法是:____________________,现象为:________;用G溶液可以腐蚀铜印刷电路板,离子反应方程式为___________________________;
(5)金属铝与A的氧化物可用来焊接火车铁轨,实验室中该反应所需药品有_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价层电子对互斥模型(VSEPR模型)的叙述中不正确的是
A. VSEPR模型可用来预测分子的立体结构
B. 分子中价电子对相互排斥决定了分子的空间结构
C. 中心原子上的孤电子对不参与互相排斥
D. 分子中键角越大,价电子对相互排斥力越小,分子越稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com