
已知酸性:H2SO4 > 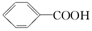 >H2CO3>
>H2CO3> 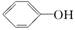 > HCO3—,综合考虑反应物的转化率和原料成本等因素,将
> HCO3—,综合考虑反应物的转化率和原料成本等因素,将 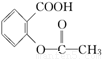 转变为
转变为
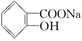 的最佳方法是(
)
的最佳方法是(
)
A.与稀H2SO4共热后,加入足量的NaOH溶液
B.与稀H2SO4共热后,加入足量的Na2CO3溶液
C.与足量的NaOH溶液共热后,再通入足量CO2
D.与足量的NaOH溶液共热后,再加入适量H2SO4
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 >H2CO3>
>H2CO3> ,将
,将 转变为
转变为 的方法是( )
的方法是( )| A、与足量的NaOH溶液共热,再通入足量的CO2 | B、与稀H2SO4共热后,加入足量的NaOH溶液 | C、加热溶液,通入足量的CO2 | D、与稀H2SO4共热后,加入足量的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知酸性:> H2CO3 >
,综合考虑反应物的转化率和原料成本等因素,将
转变为
的最佳方法是
A.与稀H2SO4共热后,加入足量的NaOH溶液
B.与稀H2SO4共热后,加入足量的Na2CO3溶液
C.与足量的NaOH溶液共热后,再通入足量CO2
D.与足量的NaOH溶液共热后,再加入适量H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com