
| A. | 向饱和CaCl2溶液中通入少量的CO2:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | 向碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| C. | 向Cu粉中加入过量的浓HNO3:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 氯化铵溶液显酸性的原因:NH4++OH-=NH3•H2O+H+ |
分析 A.盐酸酸性强于碳酸;
B.氢氧化钠过量,铵根离子与氢氧根离子也反应;
C.二者反应生成硝酸铜和二氧化氮和水;
D.铵根离子水解生成一水合氨和氢离子.
解答 解:A.盐酸酸性强于碳酸,依据强酸制备弱酸规律,氯化钙溶液与二氧化不反应,故A错误;
B.向碳酸氢铵溶液中加入过量氢氧化钠溶液,离子方程式:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故B错误;
C.向Cu粉中加入过量的浓HNO3,离子方程式:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故C正确;
D.氯化铵溶液显酸性的原因,离子方程式:NH4++H2O?NH3•H2O+H+,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确离子方程式书写方法及离子反应实质是解题关键,注意盐类水解为可逆过程,题目难度不大.


科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阴离子交换膜 | |
| C. | Y、Z、W、A元素性质均较为活泼,但其中的某些元素在自然界中仍可以游离态的形式存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,K+、Fe2+、SCN-、Br-可以大量共存 | |
| B. | 与KI溶液反应的离子方程式为Fe3++2I-═Fe2++I2 | |
| C. | 与Na2CO3溶液反应的离子方程式为2Fe3++3CO32-+3H2O═2Fe(OH)3↓+3CO2↑ | |
| D. | 与Mg(OH)2悬浊液反应的离子方程式为3OH-+Fe3+═Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
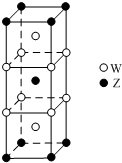 短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.
短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫的非金属性比碳强 | |
| B. | SO2气体依次通过NaHCO3溶液、澄清石灰水,澄清石灰水变浑浊 | |
| C. | SO2和CO2气体分别通入水中至饱和,测定两溶液的pH,前者小于后者 | |
| D. | 室温下测定均为0.1mol/L的NaHSO3和NaHCO3溶液的pH,前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | K2Cr2O7溶液 | Cr(OH)3 | Cr3+溶液 |
| 颜色 | 橙黄色 | 灰绿色沉淀 | 灰绿色 |
| Fe(OH)3 | Cr(OH)3 | |
| 开始沉淀时 | 1.5 | 6.0 |
| 沉淀完全时 | 2.8 | 8.0 |
| 实验 序号 | 实验装置 | 实验电压 | 溶液 | 时间 | 现象 |
| Ⅰ |  | 22V | 0.01mol/L K2Cr2O7溶液 | 20 分钟 | a 极区无明显现象; b 极区有无色气泡. |
| 实验 序号 | 实验装置 | 实验电压 | 溶液 | 时间 | 现象 |
| Ⅱ | 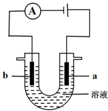 | 22V | 0.01mol/LK2Cr2O7溶液中加入少量H2SO4酸 化,使pH≈1 | 20 分钟 | a 极区溶液变浅绿色; b极区有无色气泡产生,产生红褐色沉淀. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
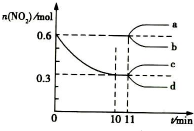 汽车尾气中CO、NO2在一定条件下可发生反应:4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200KJ/mol,一定温度下,向容积固定为 2L的密闭容器中充入一定量的 CO和 NO2,NO2 的物质的量随时间的变化曲线如图所示
汽车尾气中CO、NO2在一定条件下可发生反应:4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200KJ/mol,一定温度下,向容积固定为 2L的密闭容器中充入一定量的 CO和 NO2,NO2 的物质的量随时间的变化曲线如图所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 阿托酸属于芳香烃化合物,与苯甲酸互为同系物 | |
| B. | 阿托酸分子中至少有6个碳原子处于同一平面上 | |
| C. | 1mol阿托酸最多能和1molBr2发生加成反应 | |
| D. | 阿托酸分子能发生取代、氧化、还原以及水解等反应 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
在标准状况下,等质量的CH4 和CO2比较,下列说法中正确的是
A.密度比4:11 B.分子数之比为4:11
C.体积比4:11 D.物质的量之比为4:11
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com