
【题目】现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式 甲: 乙: C: H: 。
(2)写出反应⑦的离子方程式: ________。
(3)要除去物质F中的物质G,可行的方法是( )
A.滴入KSCN溶液 B.通入足量的氯气 C.滴入NAOH溶液 D.加入过量铁粉
(4)若将D溶液滴入F溶液中,将其长时间露置于空气中观察到的现象为_____________。
【答案】(1)H2 Cl2 Fe Fe(OH)3 (2)2Fe3++Cu=2Fe2++Cu2+
(3)D (4)有沉淀产生,沉淀颜色由白色转化为灰绿色,后继续转化为红褐色
【解析】
试题分析:黄绿色气体乙是氯气,金属A的焰色反应是显黄色,是Na,能与水反应生成气体甲和D,甲和氯气反应气体丙,则甲应该是氢气,丙是氯化氢,D是氢氧化钠。红褐色沉淀是氢氧化铁,则G是氯化铁,所以C是铁。E是盐酸,铁和盐酸反应生成氯化亚铁和氢气,则F是氯化亚铁。氯化铁和红色金属反应生成氯化亚铁,则I是铜。
(1)根据以上分析可知甲、乙、C、H的化学式分别是H2、Cl2、Fe、Fe(OH)3;
(2)⑦的离子方程式为2Fe3++Cu=2Fe2++Cu2+;
(3)铁和氯化铁反应生成氯化亚铁,则可以用铁粉除去氯化亚铁中的氯化铁,答案选D。
(4)氢氧化钠和氯化亚铁反应的实验现象是有沉淀产生,沉淀颜色由白色转化为灰绿色,后继续转化为红褐色。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在一个容积不变的密闭容器中,发生反应:2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g)
(1)当n(NO):n(O2)=4:1时,O2的转化率随时间的变化关系如下图所示。

①A点的逆反应速率v逆(O2)_____B点的正反应速率v正(O2)(填“大于”、“小于”或“等于” )。
②NO的平衡转化率为______;当达到B点后往容器中再以4:1 加入些NO和 O2,当达到新平衡时,则NO的百分含量 B点NO的百分含量(填“大于”、“小于”或“等于” )。
③到达B点后,下列关系正确的是( )
A.容器内气体颜色不再变化 B.v正(NO)=2 v正(O2)
C.气体平均摩尔质量在此条件下达到最大 D.容器内气体密度不再变化
(2)在下图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:4NO(g)+3O2(g)=2N2O5(g) △H= 。
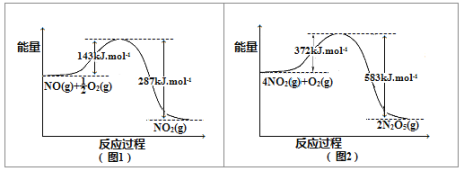

(3)降低温度,NO2(g)将转化为N2O4(g),以N2O4、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,Y为 ,有关石墨I电极反应式可表示为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体,以A和B 为原料合成扁桃酸衍生物F路线如下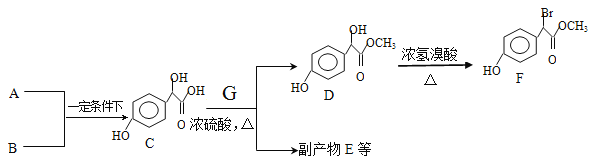
(1)根据流程图分析出G的命名 ,写出C和G反应生成D的反应方程式 。
(2)已知B为苯酚,A和B反应生成C的反应是加成反应。A可发生银镜反应,且具有酸性,则A的分子式为:_________。
(3)E是由2分子C生成的含有3个六元环的化合物,写出E的结构简式________。
(4)D→F的反应类型是__________,写出D→F的化学反应方程式 。
(5)符合下列条件的F的所有同分异构体(不考虑立体异构)的结构有 种。
①、属于一元酸类化合物,②、苯环上只有2个取代基且处于对位,其中一个是羟基
(6)A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)合成路线流程图示例如下:
合成路线的第一步已经写出,请在下面框中完成后续的合成路线流程图
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g),K1 △H1<0 (Ⅰ)
NaNO3(s)+ClNO(g),K1 △H1<0 (Ⅰ)
2NO(g)+Cl2(g)![]() 2ClNO(g),K2 △H2<0 (Ⅱ)
2ClNO(g),K2 △H2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡,测得10min内v(ClNO)=7.5×10﹣3molL﹣1min﹣1,则平衡后n(Cl2)= mol,NO的转化率α1= .其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2 α1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”“不变”)。
(3)实验室可用NaOH溶液吸收NO2,反应2NO2+2NaOH═NaNO3+NaNO2+H2O,含0.2mol NaOH水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1的CH3COONa溶液,则两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10﹣4molL﹣1,CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1)可使溶液A和溶液B的pH值相等的方法是 。
a、向溶液A中加适量水 b、向溶液A中加适量NaOH
c、向溶液B中加适量水 d、向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器A中发生反应的化学方程式为____________。
(2)装置B中的试剂是____________,若撤去装置B,可能导致装置D中副产物____________(填化学式)的量增加;装置D可采用____________加热的方法以控制反应温度在70℃左右。
(3)装置中球形冷凝管的作用为____________,写出E中所有可能发生的无机反应的离子方程式____________。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行____________。
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000molL-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000molL-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O溶液20.00mL。则产品的纯度为____________(计算结果保留三位有效数字)。
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是____________
a.分别测定0.1molL-1两种酸溶液的pH,三氯乙酸的pH较小
b.用仪器测量浓度均为0.1molL-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni和Fe在工业生产和新型材料领域有广泛的应用,黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物。室温为非活性物质。温度升高后变得活泼。在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制硫酸;回答下列问题:
(1)将FeS2与稀盐酸所对应得到H2S2,H2S2分子中,共价键的类型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是______________________;
(2)FeS2的晶体中的Fe2+离子的排列方式如下图所示:

①每个Fe2+周围最近的等距离的S22-离子有________个;
②已知FeS2的晶胞参数是a0=54nm,它的密度为_____________gcm-3;(列式并计算,阿伏加德罗常数为6.02×1023)。
(3)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为___________(用含有a的代数式表示)。在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如右图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为________g(氧离子的半径为1.40×10-10m,![]() =1.732)。
=1.732)。
查看答案和解析>>
科目:高中化学 来源: 题型:
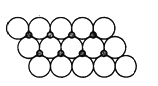
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)。


(1)写出有机物(a)的系统命名法的名称__________。
(2)有机物(a)有一种同分异构体,试写出其结构简式__________。
(3)上述有机物中与(c)互为同分异构体的是__________ (填代号).
(4)任写一种与(e)互为同系物的有机物的结构简式__________。
(5)上述有机物中不能与溴水反应但能使其褪色的有__________(填代号)。
(6) (a) (b) (c)三种物质中,4个碳原子一定处于同一平面的有________ (填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定温度下,某容积为2 L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如右图,依图所示:

(1)该反应的化学方程式是_____________________。
(2)在图上所示的三个时刻中,_______(填t1、t2或t3)时刻达到化学反应限度。
II.一定温度下将6 mol A及6 mol B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36 mol/(L·min)。求:
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36 mol/(L·min)。求:
(1)平衡时D的浓度=___________________。
(2)B的平均反应速率υ(B)= ___________________________。
(3)x=_________。
(4)开始时容器中的压强与平衡时的压强之比为______________(化为最简整数比)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成。现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g。回答下列问题:
(1)3gA中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com