
����Ŀ��������Ԫ�صĵ���X��Y��Z��ͨ��״���¾�Ϊ��̬��������ͼת����ϵ����Ӧ������ȥ������֪X��Y��Z��Ϊ˫ԭ�ӵ��ʣ�X�ǿ����к����������壬��ʹʪ��ķ�̪��ֽ��죬������ˮ�������ᡣ������������⣺
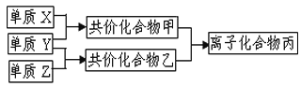
��1��X�ĵ���ʽ��_________________��
��2��д�����ҷ�Ӧ�Ļ�ѧ����ʽ__________________��
��3��ʵ���ҿ�����ͼ��ʾ��װ�ã�ȱ���ռ�װ�ã��г̶ֹ�װ����ȥ���Ʊ����ռ��ס�
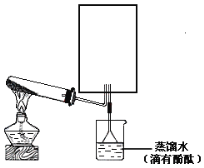
����ͼ�з����ڻ���ռ�������װ�ü�ͼ��_______________
���Թ��е��Լ���________________����д��ѧʽ����
���ձ�����Һ����ɫ��Ϊ��ɫ����ԭ���ǣ��õ��뷽��ʽ��ʾ��_________________________________��
���𰸡�![]() NH3+HCl=NH4Cl
NH3+HCl=NH4Cl  ���������֣� Ca(OH)2��NH4Cl NH3H2O NH4++OH�D
���������֣� Ca(OH)2��NH4Cl NH3H2O NH4++OH�D
��������
��֪X��Y��Z��Ϊ˫ԭ�ӵ��ʣ�X�ǿ����к����������壬��XΪ��������ʹʪ��ķ�̪��ֽ��죬���Ϊ������������ˮ�������ᣬ����ΪHCl������YΪ����������ZΪ������
��1��XΪ�����������ʽΪ![]() ��
��
��2�����ҷֱ�Ϊ������HCl�����ʱ��Ӧ�����Ȼ�泥���ѧ����ʽΪNH3+HCl=NH4Cl��
��3���ټ�Ϊ�������ܶȱȿ���С����������ˮ����ֻ���������ſ������ռ�����װ��Ϊ ��
��
��ʵ����ͨ�����Ȼ������ʯ�һ�ϼ�����ȡ�������Լ�ΪCa(OH)2��NH4Cl��
�۰�����ˮ������һˮ�ϰ�����Ϊ���ʹ��̪��Һ��죬�������笠����Ӻ����������ӣ����뷽��ʽΪNH3H2O NH4++OH�D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�Ļ�����Ʒ���ڻ�����ѧ�����У�������Ҫ�����á�
��1����������Ϊ98%���ܶ�1.84 g/cm3����Ũ������ʵ�����г�������ˮ���������ʵ���Ũ��Ϊ_________��
��2������������������Ϊ98%�����ᣬ����480 mL���ʵ���Ũ��Ϊ2.3 mol/L�����ᣬ����Ũ��������Ϊ_________ mL��
��3��ȡ�����������Ũ����ʱ�������������в������_________��
A����Һ��H2SO4�����ʵ��� B����Һ��Ũ�� C����Һ������ D����Һ���ܶ�
��4����ɣ�2����ʵ������ձ�����Ͳ���������⣬����Ҫ��������_________��
��5�����в���ʹ������Һ�����ʵ���Ũ��ƫ�ߵ�_________������ţ���
A������Ͳ��ȡŨH2SO4�����������Ų�����ע��ʢ��50 mL����ˮ��С�ձ������������ת�Ƶ�����ƿ��
B��������ƿת����Һʱ��������Һ�彦��
C��δϴ��ϡ��ŨH2SO4��С�ձ�
D������ʱ����
E������ƿδ���T����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���������������Ӧ���ǣ� ��
A | B | C | D | |
ʵ�� |
|
|
|
|
���� | һ��ʱ���a��Һ�����b��Һ�� | ����KMnO4��Һ��ɫ | pH�Ʋ�â���pH���ڢ���pH | �Թܢ����д������ݣ��Թܢ��������� |
���� | a�ܷ���������ʴ��b�ܷ������ⸯʴ | ����ϩ���ɿ���ʹ����KMnO4��Һ��ɫ | �����ԣ�Mg��Al | ���ԣ����̼����� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һЩ��ҵ�ķ�ˮ�а����������س��꣬��ˮ�ѵ��ѳ�Ϊ��Ҫ��Ⱦ����ź�ˮ�帻Ӫ�������ε��о��ȵ㣬�ж��ַ�������ȥ����
I.�����ҵ��ˮ����������ͼ��
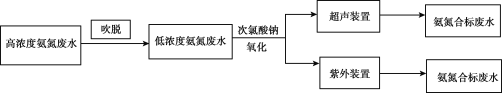
��1�����ѷ���������ˮ�еİ����������NH4+������̬��NH3����ƽ��״̬�����ڡ�������ֱ��ͨ��ˮ�У�ʹ�����Һ���ֽӴ���ˮ���ܽ�����백������Һ���棬������ת�ơ��Ӷ��ﵽ�ѳ�����Ŀ�ġ�������ˮ��NH3��NH4+ƽ��̬��ƽ���ϵ��___��
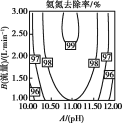
��2���¶ȡ�pHֵ�������������ѳ����кܴ��Ӱ�졣pHֵ�������������ѳ���Ӱ����ͼ��ʾ����ͼ���Կ�������������һ��ʱ��10��pH��11ʱ������������pH���Ӷ����ӣ����û�ѧƽ���ƶ�ԭ������ԭ��___��
��3���������������������ô�������������ˮ�а��������ӷ���ʽ��___��
II.���ں���H2PO4-�İ�����ˮ�������õ绯ѧ��������������Эͬȥ��ˮ�еİ�����װ����ͼ��ʾ���������У�ʯīձ�缫����OH-����ͨ��O2��������ֲ���H2O2��������ˮ�е�NH4+��ͬʱNH4+������ͨ������MgNH4PO46H2O��������������ȥ��
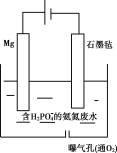
��1�������ĵ缫��Ӧʽ��___��
��2����ˮ�е�NH4+'ת��ΪMgNH4PO46H2O�����ӷ���ʽ��___��
��3��pH����10.5������MgNH4PO46H2O�����ɣ�ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ����仯���˵������ȷ����
A.�����ǿ����к�����ߵ����壬���ʱȽ��ȶ�
B.�˹��̵���Ҫ�ڸ��¸�ѹ�����������½��У������Ǹ����ȷ�Ӧ
C.��ҵ���������ᷢ�ƣ���Ϊ���к���Fe3+
D.�����£�Ũ�����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������LiOH������������Ʊ�����ӵ���������ϡ����õ��LiCl��Һ�Ʊ�LiOH��װ����ͼ��ʾ������˵����ȷ����

A.���Ե缫B������
B.��������Ϊa��A��B��b
C.�õ����õĽ���Ĥ�������ӽ���Ĥ
D.���������ĵ缫��Ӧ����ʽ��4OH- - 4e-=O2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��������������������a�г���NO2(g)����ɫ���ٱ仯����������b�г�����������ʹ����������ɫ�������ȡ�ע�⣺ͬŨ�ȵ�NO2��Br2������ɫ��ͬ��2NO2(g)![]() N2O4(g)(��ɫ)��Ѹ�ٽ�������ͬʱѹ��(�������岻Һ��)������˵����ȷ����
N2O4(g)(��ɫ)��Ѹ�ٽ�������ͬʱѹ��(�������岻Һ��)������˵����ȷ����

A.a��a�������У���ɫͻȻ���Ȼ����dz��������ɫ��ԭ����dz
B.����a��b�Լ������ٶȻ���ѹ������a��b����ɫ�������������ÿһ����ͬ��ʱ��㣬b����ɫ�ܱ�a����
C.���������ͻ�����Ϊ��ɫ�����������۲�a��a����a������ɫ��adz
D.��������ʵ�����naһ������nb��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦFeO(s)��CO(g) Fe(s)��CO2(g)��700 ��ʱƽ�ⳣ��Ϊ0.68��900��ʱƽ�ⳣ��Ϊ0.46������˵����ȷ����
A. �����¶ȸ÷�Ӧ������Ӧ���������淴Ӧ���ʼ�С
B. �÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ��![]()
C. ����CO2Ũ�ȣ�ƽ�ⳣ������
D. �÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
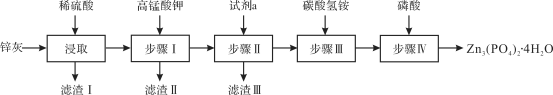
����Ŀ����ˮ������п[Zn3(PO4)2��4H2O��Ħ������Ϊ457 g��mol��1��������ˮ] ��һ��������������ɫ�����������ϡ�ʵ������п�ң���ZnO��PbO��CuO��FeO��Fe2O3��SiO2�ȣ�Ϊԭ���Ʊ�Zn3(PO4)2��4H2O���������£��ش��������⣺
��֪��6NH4HCO3 + 3ZnSO4 ![]() ZnCO3��2Zn(OH)2��H2O�� + 3(NH4)2SO4 + 5CO2��
ZnCO3��2Zn(OH)2��H2O�� + 3(NH4)2SO4 + 5CO2��
ZnCO3��2Zn(OH)2��H2O + 2H3PO4 ![]() Zn3(PO4)2��4H2O + 2H2O + CO2��
Zn3(PO4)2��4H2O + 2H2O + CO2��
��1�����������Ҫ�ɷ�Ϊ________��������У����Ƚ���Һ��pH����5.1����ʱӦѡ�������Լ���________��
a����ˮ b���������� c������п d����������
�μ�KMnO4��Һ����MnO2���ɣ��÷�Ӧ�����ӷ���ʽΪ________���Լ�aΪ________���������Ӧ�����õ�Zn3(PO4)2��4H2O�IJ�������________���
��2����ȡ45.7 mg Zn3(PO4)2��4H2O�������ط������������������¶ȵı仯��ϵ��ͼ��ʾ��Ϊ���Zn3(PO4)2��2H2O��Zn3(PO4)2��H2O�Ļ�ϲ�Ʒ�����ʱ���¶ȷ�ΧΪ________��
a��90��145�� b��145��195�� c��195��273�� d����273��

��3��Ϊ�ⶨ��Ʒ��Zn3(PO4)2��4H2O�ĺ�������������ʵ�飬��֪�ζ�������Zn2+��H2Y2��1:1��Ӧ��
�����ȷ��ȡ0.4570 g��Ʒ���ձ��У�������������ʹ���ܽ⣬����Һת����100 mL����ƿ�����ݡ�
�������ȡ20.00 mL������Һ����ƿ�У�����ָʾ������pH = 5��6�Ļ�����Һ����0.02000mol��L��1 Na2H2Y����Һ�ζ����յ㣬���Na2H2Y����Һ������Ϊ27.60 mL��
���������ȡ��Һʱ��ʹ�õIJ�������Ϊ________����Ʒ��Zn3(PO4)2��4H2O����������Ϊ_______�����в����У����²�Ʒ��Zn3(PO4)2��4H2O�����ⶨֵƫ�͵���________��
a������I�ж���ʱ���ӿ̶���
b������I��ת����Һʱδϴ���ձ�
c������II�еζ���δ��Na2H2Y����Һ��ϴ
d������II�еζ�ǰ�ζ����������ݣ��ζ�������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com