
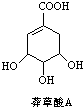
 为原料的有机合成路线:
为原料的有机合成路线:
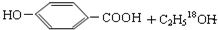 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$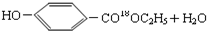 .
. .
. 分析 草莽酸A与B发生酯化反应,根据草莽酸A的结构简式可知其含有羟基和羧基,可与酸羧酸或醇发生酯化反应,根据C的相对分子质量可知,B可以为CH3CH2OH或HCOOH,D遇氯化铁变紫色,说明D中含有酚羟基,D的核磁共振氢谱中有4组峰,则D应为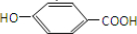 ,D与乙醇发生酯化反应得E为
,D与乙醇发生酯化反应得E为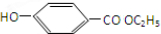 ,据此答题;
,据此答题;
解答 解:草莽酸A与B发生酯化反应,根据草莽酸A的结构简式可知其含有羟基和羧基,可与酸羧酸或醇发生酯化反应,根据C的相对分子质量可知,B可以为CH3CH2OH或HCOOH,D遇氯化铁变紫色,说明D中含有酚羟基,D的核磁共振氢谱中有4组峰,则D应为 ,D与乙醇发生酯化反应得E为
,D与乙醇发生酯化反应得E为 ,
,
(1)根据草莽酸A的结构简式可知其含有羟基和羧基,
故答案为:羟基和羧基;
(2)每个莽草酸A中含有一个羧基,所以1mol莽草酸A最多能和1molNaOH发生反应,
故答案为:1;
(3)根据上面的分析可知,B可能的结构简式为CH3CH2OH或HCOOH,
故答案为:CH3CH2OH或HCOOH;
(4)反应D→E的化学方程式为: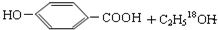 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$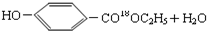 ,
,
故答案为: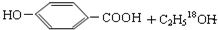 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$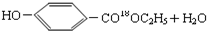 ;
;
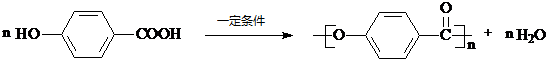
(5)在一定条件下D自身聚合成一种高分子材料,其反应的方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的合成与推断,侧重于学生的分析能力的考查,为高频考点,注意把握有机物的结构和官能团的性质,为解答该题的关键,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
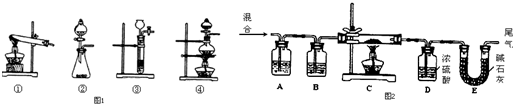
 用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 常温下,c(H+)/c(OH-)=1010的溶液中:Na+、NH4+、ClO-、I- | |
| C. | 水电离出的c(H+)=10-12mol•L-1的溶液:K+、Na+、CO32-、Br- | |
| D. | 含有0.1mol•LHCO3-的溶液:Na+、Fe3+、NO3-、SCN- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com