
ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ(””””)
A£®ĒŠæŖµÄ½šŹōNa±©Ā¶ŌŚæÕĘųÖŠ£¬¹āĮĮµÄ±ķĆęÖš½„±ä°µ£¬·¢ÉśµÄ·“Ó¦ĪŖ2Na£«O2===Na2O2
B£®4.6 g NaÓėO2ĶźČ«·“Ó¦£¬Éś³É7 g²śĪļŹ±Ź§Č„µē×ÓµÄĪļÖŹµÄĮæĪŖ0.2 mol
C£®NaÓėĻ”ĮņĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Na£«2H£«===2Na£«£«H2”ü
D£®½«ÉŁĮæNaĶ¶Čėµ½CuSO4ČÜŅŗÖŠ£¬¼ČÓŠ³ĮµķÉś³ÉÓÖÓŠĘųĢå·Å³ö
“š°ø””A
½āĪö””AĻī“ķ£¬³£ĪĀĻĀĒŠæŖµÄ½šŹōNa±©Ā¶ŌŚæÕĘųÖŠ£¬¹āĮĮµÄ±ķĆęÖš½„±ä°µŹĒŅņĪŖÉś³ÉNa2O£»BĻīÕżČ·£¬ÓÉĢāŅāÖŖĖäȻɜ³ÉNa2O2ŗĶNa2OµÄ»ģŗĻĪļ£¬µ«ŹĒNaµÄĪļÖŹµÄĮæĪŖ0.2 mol£¬¹ŹŹ§Č„µē×ÓµÄĪļÖŹµÄĮæČŌĪŖ0.2 mol£»CĻīÕżČ·£¬NaÓėĻ”H2SO4·“Ó¦µÄ±¾ÖŹŹĒÓėH£«µÄ·“Ó¦£¬H2SO4ŹĒĒæĖį£»DĻīÕżČ·£¬NaÓėĖ®·“Ó¦·Å³öĘųĢå£¬Éś³ÉµÄNaOHÓėĮņĖįĶ·“Ӧɜ³ÉĒāŃõ»ÆĶ³Įµķ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ³żČ„ŌÓÖŹµÄ·½·Ø²»ÕżČ·µÄŹĒ (””””)”£
A£®Ć¾·ŪÖŠ»ģÓŠÉŁĮæĀĮ·Ū£ŗ¼ÓČė¹żĮæÉÕ¼īČÜŅŗ³ä·Ö·“Ó¦£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ
B£®ÓĆ¹żĮæ°±Ė®³żČ„Fe3£«ČÜŅŗÖŠµÄÉŁĮæAl3£«
C£®ÓĆŠĀÖʵÄÉśŹÆ»Ņ£¬Ķعż¼ÓČČÕōĮó£¬ŅŌ³żČ„ŅŅ“¼ÖŠµÄÉŁĮæĖ®
D£®Al(OH)3ÖŠ»ģÓŠÉŁĮæMg(OH)2£ŗ¼ÓČė×ćĮæÉÕ¼īČÜŅŗ£¬³ä·Ö·“Ó¦£¬¹żĀĖ£¬ĻņĀĖŅŗÖŠĶØČė¹żĮæCO2ŗó¹żĀĖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijČÜŅŗÖŠŗ¬ÓŠHCO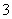 ”¢SO
ӢSO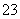 ӢCO
”¢CO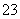 ”¢CH3COO£4ÖÖŅõĄė×Ó”£ĻņĘäÖŠ¼ÓČė×ćĮæµÄNa2O2¹ĢĢåŗó£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č»ł±¾±£³Ö²»±äµÄŹĒ(¼ŁÉčČÜŅŗĢå»żĪŽ±ä»Æ)(””””)
”¢CH3COO£4ÖÖŅõĄė×Ó”£ĻņĘäÖŠ¼ÓČė×ćĮæµÄNa2O2¹ĢĢåŗó£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č»ł±¾±£³Ö²»±äµÄŹĒ(¼ŁÉčČÜŅŗĢå»żĪŽ±ä»Æ)(””””)
A£®CH3COO£ B£®SO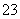
C£®CO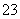 D£®HCO
D£®HCO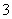
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÄʵĻ¹ŌŠŌ±Č¼ŲµÄČõ£¬µ«¹¤ŅµÉĻÖĘČ”¼ŲČ“ÓĆÄĘÖĆ»»¼ŲµÄŌŅņŹĒ_________________
________________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ(””””)
A£®NaHCO3ČÜŅŗÖŠ¼ÓČėĻ”HCl£ŗCO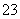 £«2H£«===CO2”ü£«H2O(2014·ĖÄ“ØĄķ×Ū£¬3B)
£«2H£«===CO2”ü£«H2O(2014·ĖÄ“ØĄķ×Ū£¬3B)
B. Ģ¼ĖįÄĘČÜŅŗĻŌ¼īŠŌ£ŗCO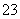 £«H2O??HCO
£«H2O??HCO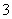 £«OH£(2013·±±¾©Ąķ×Ū£¬8B)
£«OH£(2013·±±¾©Ąķ×Ū£¬8B)
C£®Na2O2ČÜÓŚĖ®²śÉśO2£ŗNa2O2£«H2O===2Na£«£«2OH££«O2”ü(2013·½ĖÕ£¬8C)
D£®Ģ¼ĖįĒāÄĘČÜŅŗÖŠµĪČėĒāŃõ»ÆøĘČÜŅŗ£ŗHCO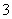 £«OH£===CO
£«OH£===CO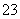 £«H2O(2012·ŗ£ÄĻ£¬12A)
£«H2O(2012·ŗ£ÄĻ£¬12A)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¼ī½šŹōīÕ(Fr)¾ßÓŠ·ÅÉäŠŌ£¬ĖüŹĒ¼ī½šŹōŌŖĖŲÖŠ×īÖŲµÄŌŖĖŲ£¬øł¾Ż¼ī½šŹōŌŖĖŲŠŌÖŹµÄµŻ±ä¹ęĀÉŌ¤²āĘäŠŌÖŹ£¬ĘäÖŠ²»ÕżČ·µÄŹĒ(””””)
A£®ŌŚ¼ī½šŹōŌŖĖŲÖŠĖü¾ßÓŠ×ī“óµÄŌ×Ó°ė¾¶
B£®īÕŌŚæÕĘųÖŠČ¼ÉÕŹ±£¬Ö»Éś³É»ÆѧŹ½ĪŖFr2OµÄŃõ»ÆĪļ
C£®ĖüµÄĒāŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖFrOH£¬ÕāŹĒŅ»ÖÖ¼«ĒæµÄ¼ī
D£®ĖüÄÜøśĖ®·“Ӧɜ³ÉĻąÓ¦µÄ¼īŗĶĒāĘų£¬ÓÉÓŚ·“Ó¦¾ēĮŅ¶ų·¢Éś±¬ÕØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ±ķŹ¾Ź½“ķĪóµÄŹĒ(””””)
A£®Na£«µÄ¹ģµĄ±ķŹ¾Ź½£ŗ B£®Na£«µÄ½į¹¹Ź¾ŅāĶ¼£ŗ
B£®Na£«µÄ½į¹¹Ź¾ŅāĶ¼£ŗ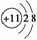
C£®NaµÄµē×ÓÅŲ¼Ź½£ŗ1s22s22p63s1 D£®NaµÄ¼ņ»Æµē×ÓÅŲ¼Ź½£ŗ[Ne]3s1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¾ŻĻĀĮŠŠšŹö£¬Š“³öŌŖĖŲĆū³ĘŗĶŗĖĶāµē×ÓÅŲ¼Ź½”£
(1)AŌŖĖŲŌ×ÓŗĖĶāM²ćµē×ÓŹżŹĒL²ćµē×ÓŹżµÄŅ»°ė£ŗ___________”£
(2)BŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ1.5±¶£ŗ________________”£
(3)CŌŖĖŲµÄµ„ÖŹŌŚ³£ĪĀĻĀæÉÓėĖ®¾ēĮŅ·“Ó¦£¬²śÉśµÄĘųĢåÄÜŹ¹“ų»šŠĒµÄľĢõø“Č¼£ŗ________________________________________”£
(4)DŌŖĖŲµÄ“ĪĶā²ćµē×ÓŹżŹĒ×īĶā²ćµē×ÓŹżµÄ1/4£ŗ__________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ō×ÓŠĪ³É»ÆŗĻĪļŹ±£¬µē×ÓŌĘ¼äµÄĻą»„×÷ÓƶŌĪļÖŹµÄ½į¹¹ŗĶŠŌÖŹ»į²śÉśÓ°Ļģ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)BF3·Ö×ÓµÄĮ¢Ģå½į¹¹ĪŖ______________£¬NF3·Ö×ÓµÄĮ¢Ģå½į¹¹ĪŖ____________”£
(2)Ģ¼Ō×ÓÓŠ4øö¼Ūµē×Ó£¬ŌŚŠĪ³É»ÆŗĻĪļŹ±¼Ūµē×Ó¾ł²ĪÓė³É¼ü£¬µ«ŌӻƷ½Ź½²»Ņ»¶ØĻąĶ¬”£ŌŚŅŅĶ锢ŅŅĻ©”¢ŅŅČ²ŗĶ±½ĖÄÖÖ·Ö×ÓÖŠ£¬Ģ¼Ō×Ó²ÉČ”spŌӻƵķÖ×ÓŹĒ____________(Š“½į¹¹¼ņŹ½£¬ĻĀĶ¬)£¬²ÉČ”sp2ŌӻƵķÖ×ÓŹĒ__________£¬²ÉČ”sp3ŌӻƵķÖ×ÓŹĒ____________”£ŹŌŠ“³öŅ»ÖÖÓŠ»śĪļ·Ö×ӵĽį¹¹¼ņŹ½£¬ŅŖĒóĶ¬Ź±ŗ¬ÓŠČżÖÖ²»Ķ¬ŌӻƷ½Ź½µÄĢ¼Ō×Ó£ŗ________________________________________________________________________”£
(3)ŅŃÖŖH2O”¢NH3”¢CH4ČżÖÖ·Ö×ÓÖŠ£¬¼ü½ĒÓɓ󵽊”µÄĖ³ŠņŹĒCH4>NH3>H2O£¬Ēė·ÖĪöæÉÄܵÄŌŅņŹĒ________________________________________________”£
(4)ÓÉÓŚµēŗɵÄ×÷ÓĆ£¬Ņõ”¢ŃōĄė×ÓŠĪ³É»ÆŗĻĪļŹ±Ąė×ӵĵē×ÓŌĘ»į·¢Éś±ä»Æ£¬Ź¹Ąė×Ó¼üÖš½„Ļņ¹²¼Ū¼ü¹ż¶É”£ŃōĄė×ÓµēŗÉŹżŌ½¶ą£¬ŅõĄė×Ó°ė¾¶Ō½“óŹ±£¬µē×ÓŌʱä»ÆŌ½“󣬵¼ÖĀĖłŠĪ³ÉµÄ»ÆŗĻĪļŌŚĖ®ÖŠµÄČܽā¶ČŌ½Š””£ÓÉ“ĖæÉÖŖ£¬ĖÄÖÖĀ±»ÆŅų(AgF”¢AgCl”¢AgBrŗĶAgI)ŌŚĖ®ÖŠµÄČܽā¶ČÓɓ󵽊”µÄĖ³ŠņĪŖ________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com