
| A. | ①②③ | B. | ①②⑤ | C. | ②④⑤ | D. | ②③⑤ |
分析 溶液呈黄色的原因可能是稀溴水的颜色,也可能是氯化铁溶液呈现的黄色,若加入有机溶剂,采用物理方法检验溴单质;若使用硫氰化钾溶液检验Fe3+的存在,结合给出的试剂可知,阴离子与硝酸银生成沉淀不同,铁离子与碱反应生成红褐色沉淀,以此来解答.
解答 解:①二者均与氯水不反应,不能鉴别,故不选;
②氯化铁与硝酸银溶液反应生成白色沉淀,而溴水与硝酸银生成浅黄色沉淀,可鉴别,故选;
③二者均与淀粉溶液不反应,不能鉴别,故不选;
④氯化铁与氢氧化钠溶液反应生成红褐色沉淀,溴水与NaOH反应得到无色溶液,故选;
⑤溴水与四氯化碳混合下层呈橙红色,而氯化铁与与四氯化碳混合下层为无色,故选;
故选C.
点评 本题考查物质的检验和鉴别,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:2:4 | B. | 1:2:3 | C. | 3:2:1 | D. | 2:5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S与SO2、NO与O2、NH3与HCl在常温下均不能大量共存 | |
| B. | (NH4)2SO3、Ca(ClO)2、NaAlO2均既能和稀硫酸又能和氢氧化钠溶液反应 | |
| C. | Fe(OH)3、FeCl2、FeCl3、NO均可通过化合反应得到 | |
| D. | AlCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NaOH溶液鉴别(NH4)2SO4和NH4Cl | |
| B. | 用AgNO3溶液鉴别NaBr溶液和KI溶液 | |
| C. | 用焰色反应鉴别NaCl和NaNO3 | |
| D. | 用澄清石灰水鉴别CO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
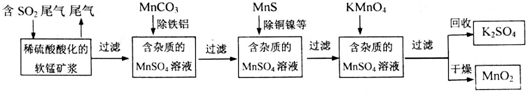
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23gNa在氧气中完全燃烧失电子数为0.5NA | |
| B. | 1mol NO和1mol O2的混合气体中含有的分子数为2NA | |
| C. | 标准状况下,11.2L SO3所含分子数为0.5NA | |
| D. | 1.5mol NO2与足量H2O反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH(CH3)2属于链状化合物 | B. | 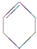 属于芳香化合物 属于芳香化合物 | ||
| C. |  属于脂环化合物 属于脂环化合物 | D. |  属于芳香化合物 属于芳香化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①③⑤⑦ | C. | ②④⑥⑦ | D. | ①⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com