
【题目】25℃时,有c(HA)+c(A-)=0.1mol/L的一组HA、KA混合溶液,溶液中c(HA)、c(A-)与pH的关系如下图所示。下列叙述不正确的是 ( )
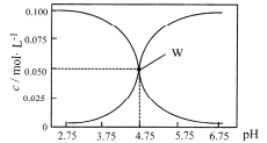
A.pH=5.75的溶液中:c(K+)>c(A-)>c(HA)> c (H+)>c(OH-)
B.欲得W点所示溶液,起始所加溶液应符合c(HA)+c(A-)=0.1mol/L且c(KA)<c(HA)
C.pH=3.75的溶液中:c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L
D.若A-的水解常数为Kh,则lgKh=-9.25
【答案】A
【解析】
A. pH=5.75的溶液显酸性,HA的电离程度大于A-的水解程度;
B. W点的溶液中c(HA)= c(A-),酸的电离程度大于A-的水解程度,欲得W点所示溶液且满足c(HA)+c(A-)=0.1mol/L据此计算;
C. pH=3.75的溶液中存在电荷守恒,结合c(HA)+c(A-)=0.1mol/L进行计算;
D. A-+H2O![]() HA+OH-,Kh=
HA+OH-,Kh=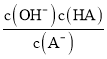 =
=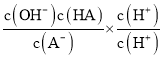 =
=![]() ,当pH=4.75时,c(HA)= c(A-),结合Ka=
,当pH=4.75时,c(HA)= c(A-),结合Ka=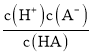 = c(H+)进行计算。
= c(H+)进行计算。
A. pH=5.75的溶液显酸性,HA的电离程度大于A-的水解程度,因此溶液浓度的大小关系为:c(A-) > c(K+) >c(HA)> c (H+)>c(OH-),A项错误,符合题意;
B. W点的溶液中c(HA)= c(A-),酸的电离程度大于A-的水解程度,欲得W点所示溶液满足c(HA)+c(A-)=0.1mol/L且c(KA)>c(HA),才能满足c(HA)= c(A-),B项正确,不符合题意;
C. pH=3.75的溶液中存在电荷守恒:c(K+)+c(H+)=c(OH-)+c(A-),又c(HA)+c(A-)=0.1mol/L,因此c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L,C项正确,不符合题意;
D. 当pH=4.75时,c(HA)= c(A-),Ka=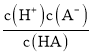 = c(H+)=10-4.75mol/L,因此Kh=
= c(H+)=10-4.75mol/L,因此Kh=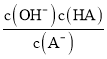 =
=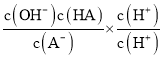 =
=![]() =
=![]() =10-9.25,所以lgKh=-9.25,D项正确,不符合题意;
=10-9.25,所以lgKh=-9.25,D项正确,不符合题意;
答案选A。


科目:高中化学 来源: 题型:
【题目】砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措施之一。
(1)将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有![]() ,其原因是_______________________________。
,其原因是_______________________________。
(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题20图- 1和题20图- 2所示。
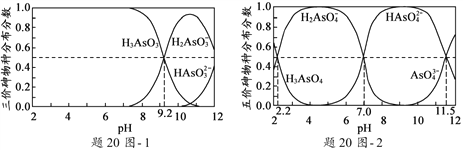
①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________。
②H3AsO4第一步电离方程式H3AsO4![]() H2AsO4-+H+的电离常数为Ka1,则pKa1=______(p Ka1 = -lg Ka1 )。
H2AsO4-+H+的电离常数为Ka1,则pKa1=______(p Ka1 = -lg Ka1 )。
(3)溶液的pH对吸附剂X表面所带电荷有影响。pH =7.1时, 吸附剂X表面不带电荷; pH > 7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如题20图-3所示。

①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是______________。
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为___________。 提高吸附剂X对三价砷去除效果可采取的措施是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(化学名称为乙酰水杨酸)是具有解毒、镇痛等功效的家庭常备药,科学家用它连接在高分子载体上制成缓释长效阿司匹林,其部分合成过程如下:

已知:醛或酮均可发生下列反应:CH3CHO ![]()
(1)水杨酸的化学名称为邻羟基苯甲酸,则水杨酸的结构简式为__;
(2)反应Ⅰ的反应类型是__反应.HOCH2CH2OH可由1,2﹣二溴乙烷制备,实现该制备所需的反应试剂是__;
(3)写出C→D的反应方程式______;
(4)C可发生缩聚反应生成高聚物,该高聚物的结构简式为____;
(5)阿司匹林与甲醇酯化的产物在氢氧化钠溶液中充分反应的化学方程式为______;
(6)下列说法正确的是__;
a.服用阿司匹林出现水杨酸中毒,应立即停药,并静脉注射NaHCO3溶液
b.1mol HOCH2CH2OH的催化氧化产物与银氨溶液反应,理论上最多生成2mol银
c.A的核磁共振氢谱只有一组峰
d.两分子C发生酯化反应可生成8元环状酯
(7)写出缓释阿司匹林在体内水解生成阿司匹林、高聚物E等物质的反应方程式__;
(8)水杨酸有多种同分异构体,其中属于酚类且能发生银镜反应的同分异构体有__种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,其结构简式如图所示。下列有关叙述中正确的是()

A.遇FeCl3溶液不能发生显色反应
B.可与NaOH和NaHCO3溶液发生反应
C.1mol该有机物可以与5molBr2发生反应
D.己烯雌酚分子中一定有16个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,其结构简式如图所示。下列说法不正确的是( )
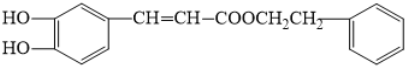
A. CPAE能发生取代反应、加成反应
B. CPAE能使酸性高锰酸钾溶液褪色
C. CPAE可与氢氧化钠溶液发生反应
D. CPAE在酸性条件下水解得到相对分子质量较小的有机物的同分异构体共有9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇与氢卤酸反应是制备卤代烃的重要方法。已知:溴乙烷及1-溴丁烷均难溶于水且二者在氢氧化钠作用下会发生水解反应。实验室制备溴乙烷和 1溴丁烷的反应如下:
NaBr+H2SO 4 =HBr+NaHSO4 ①
R—OH+HBr→ R—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br- 被浓硫酸氧化为 Br2等。有关数据列表如下:

请回答下列问题:
(1)在蒸馏过程中,仪器选择及安装都正确的是____________(填标号)。

(2)醇的水溶性______(填“大于”、“等于”或“小于”)相应的溴代烃。
(3)将 1溴丁烷粗产品置于分液漏斗中加水,振荡后静置,水在________(填“上层”“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的是________(填字母)。
a.水是反应的催化剂 b.减少 Br2 的生成
c.减少 HBr 的挥发 d.减少副产物烯和醚的生成
(5)欲除去溴乙烷中的少量杂质 Br 2 ,下列物质中最适合的是________(填字母)。
a.NaI b.KCl c.NaOH d.NaHSO 3
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于_______;但在制备 1溴丁烷时却不能边反应边蒸出产物,其原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际奥委会公布的违禁药物有138种,其中某种兴奋剂分子结构如图,关于它的说法正确的是( )

A. 该物质属于芳香烃
B. 该分子中所有碳原子共面
C. 1mol该物质与氢氧化钠溶液完全反应,最多消耗2molNaOH
D. 该物质的化学式为C15H24ClNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是
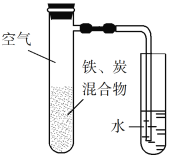
A. 铁被氧化的电极反应式为Fe3e![]() Fe3+
Fe3+
B. 铁腐蚀过程中化学能全部转化为电能
C. 活性炭的存在会加速铁的腐蚀
D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com