
ĻĀ±ķŹĒ¼øÖÖÄŃČÜĪļÖŹµÄÓŠ¹ŲŹżÖµ£ŗ
| ĪļÖŹ | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25 ”ę | 8.0”Į10£16 | 2.2”Į10£20 | 4.0”Į10£36 |
| ĶźČ«³ĮµķŹ±µÄpH·¶Ī§ | ”Ż9.6 | ”Ż6.4 | ”Ż3 |
¹ŲÓŚŗ¬µČĪļÖŹµÄĮæµÄCuSO4”¢FeSO4”¢Fe2(SO4)3µÄ»ģŗĻČÜŅŗµÄĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ (””””)”£
A£®ĻņøĆ»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ£¬×īĻČÉś³ÉµÄ³ĮµķŹĒĄ¶É«µÄ
B£®øĆČÜŅŗÖŠc(SO )”Ć[c(Cu2£«)£«c(Fe2£«)£«c(Fe3£«)]>5”Ć4
)”Ć[c(Cu2£«)£«c(Fe2£«)£«c(Fe3£«)]>5”Ć4
C£®µ±pH£½10Ź±£¬ČÜŅŗÖŠc(Fe2£«)”Ćc(Fe3£«)£½(2”Į1020)”Ć1
D£®ĻņøĆČÜŅŗÖŠ¼ÓČėŹŹĮæ°±Ė®£¬µ÷½ŚpHµ½9.6ŗó¹żĀĖ½«ĖłµĆ³Įµķ×ĘÉÕ£¬æɵƵČĪļÖŹµÄĮæµÄCuO”¢FeO
½āĪö””Ķعż±ķÖŠŹż¾Ż¼ĘĖćæÉÖŖæŖŹ¼Éś³É³ĮµķŹ±£¬Fe(OH)3 ĖłŠčc(OH£)×īŠ”£¬¹Ź×īĻČÉś³ÉµÄ³ĮµķŹĒŗģŗÖÉ«µÄFe(OH)3£¬A“ķĪó£»ÓɽšŹōŃōĄė×ÓÄÜĖ®½ā¶ųSO ²»ÄÜĖ®½āæÉÖŖ£¬BÕżČ·£»µ±pH£½10Ź±£¬c(Fe2£«)”Ćc(Fe3£«)£½(8”Į10£16”Ā
²»ÄÜĖ®½āæÉÖŖ£¬BÕżČ·£»µ±pH£½10Ź±£¬c(Fe2£«)”Ćc(Fe3£«)£½(8”Į10£16”Ā
10£8)”Ć(4”Į10£36”Ā10£12)£½(2”Į1016)”Ć1£¬C“ķĪó£»Éś³ÉµÄFe(OH)2²»ĪČ¶Ø£¬»įČ«²æ×Ŗ»ÆĪŖFe(OH)3£¬¹Ź×īŗóµĆµ½µÄ¹ĢĢå֊ƻӊFeO£¬D“ķĪó”£
“š°ø””B


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĢžA 0.2 molŌŚŃõĘųÖŠ³ä·ÖČ¼ÉÕŗó£¬Éś³É»ÆŗĻĪļB”¢Cø÷1.2 mol£¬ŹŌ»Ų“š£ŗ
(1)ĢžAµÄ·Ö×ÓŹ½ŹĒ________”£
(2)ČōČ”Ņ»¶ØĮæµÄĢžA³ä·ÖČ¼ÉÕŗó£¬Éś³ÉB”¢Cø÷3 mol£¬ŌņÓŠ________gµÄA²Ī¼ÓĮĖ·“Ó¦£¬Č¼ÉÕŹ±Ļūŗıź×¼×“æöĻĀµÄŃõĘų________L”£
(3)ČōĢžAÄÜŹ¹äåĖ®ĶŹÉ«£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀÓėH2·¢Éś¼Ó³É·“Ó¦ŗóÉś³É2,2¶ž¼×»ł¶”Ķ飬ŌņĢžAµÄĆū³ĘŹĒ________________£¬½į¹¹¼ņŹ½ŹĒ________________”£
(4)±ČAÉŁĮ½øöĢ¼Ō×ÓµÄAµÄĻ©ĢžĶ¬ĻµĪļµÄĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ____________ÖÖ£¬ĘäÖŠÖ»ŗ¬ÓŠŅ»øö¼×»łµÄ½į¹¹¼ņŹ½ĪŖ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ŲÓŚ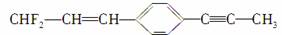 µÄ·Ö×Ó½į¹¹Ėµ·ØÕżČ·µÄŹĒ(””””)
µÄ·Ö×Ó½į¹¹Ėµ·ØÕżČ·µÄŹĒ(””””)
A£®·Ö×ÓÖŠ12øöĢ¼Ō×ÓŅ»¶ØŌŚĶ¬Ņ»Ę½Ćę
B£®·Ö×ÓÖŠÓŠ7øöĢ¼Ō×ÓæÉÄÜŌŚĶ¬Ņ»Ö±ĻßÉĻ
C£®·Ö×ÓÖŠ×ī¶ąÓŠ6øöĢ¼Ō×ÓÄÜŌŚĶ¬Ņ»Ö±ĻßÉĻ
D£®·Ö×ÓÖŠ×ī¶ąÓŠ8øöĢ¼Ō×ÓÄÜŌŚĶ¬Ņ»Ö±ĻßÉĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬Ļņ20 mL 0.2 mol”¤L£1 H2AČÜŅŗÖŠµĪ¼Ó0.2 mol”¤L£1 NaOHČÜŅŗ”£ÓŠ¹ŲĪ¢Į£µÄĪļÖŹµÄĮæ±ä»ÆĒéæöČēĶ¼ĖłŹ¾(ĘäÖŠ¢ń“ś±ķH2A£¬¢ņ“ś±ķHA££¬¢ó“ś±ķA2£)”£øł¾ŻĶ¼Ź¾ÅŠ¶Ļ£¬µ±V(NaOH)£½20 mLŹ±£¬ČÜŅŗÖŠø÷Į£×ÓÅØ¶ČµÄ“óŠ”Ė³ŠņÕżČ·µÄŹĒ (””””)”£
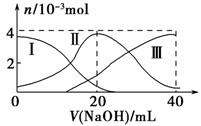
A£®c(Na£«)>c(HA£)>c(OH£)>c(H2A)>c(H£«)>c(A2£)
B£®c(Na£«)>c(HA£)>c(H£«)>c(A2£)>c(H2A)>c(OH£)
C£®c(Na£«)>c(H£«)>c(HA£)>c(A2£)>c(OH£)>c(H2A)
D£®c(Na£«)>c(OH£)>c(HA£)>c(H2A)>c(H£«)>c(A2£)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ»ÆѧŌĄķµÄÓ¦ÓĆ£¬Ö÷ŅŖÓĆ³ĮµķČܽāĘ½ŗāŌĄķĄ“½āŹĶµÄŹĒ (””””)”£
¢ŁČČ“æ¼īČÜŅŗČ„ÓĶĪŪÄÜĮ¦Ēæ
¢ŚĪ󽫱µŃĪ[BaCl2”¢Ba(NO3)2]µ±×÷Ź³ŃĪ»ģÓĆŗ󣬳£ÓĆ0.5%µÄNa2SO4ČÜŅŗ½ā¶¾
¢ŪČܶ“”¢Éŗŗ÷µÄŠĪ³É
¢ÜĢ¼Ėį±µ²»ÄÜ×÷”°±µ²Ķ”±¶ųĮņĖį±µŌņÄÜ
¢ŻÅŻÄĆš»šĘ÷Ćš»šµÄŌĄķ
A£®¢Ś¢Ū¢Ü”” B£®¢Ł¢Ś¢Ū
C£®¢Ū¢Ü¢Ż”” D£®¢Ł¢Ś¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪŖĮĖ½ųŅ»²½ĢįøßŗĻ³É°±µÄÉś²śŠ§ĀŹ£¬æĘŃŠÖŠ¾ßÓŠæŖ·¢¼ŪÖµµÄŹĒ (””””)”£
A£®ŃŠÖĘøßĪĀĻĀ»īŠŌ½Ļ“óµÄ“߻ƼĮ
B£®Ń°ĒóNH3µÄŠĀĄ“Ō“
C£®ŃŠÖʵĶĪĀĻĀ»īŠŌ½Ļ“óµÄ“߻ƼĮ
D£®ŃŠÖĘÄĶøßĪĀøßŃ¹µÄŠĀŠĶ²ÄĮĻ½ØŌģŗĻ³ÉĖž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ唣¶ŌÓŚĆܱÕČŻĘ÷ÖŠµÄ·“Ó¦£ŗN2(g)£«3H2(g)2NH3(g)£¬673 K”¢30 MPaĻĀn(NH3)ŗĶn(H2)Ėꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ (””””)”£

A£®µćaµÄÕż·“Ó¦ĖŁĀŹ±ČµćbµÄŠ”
B£®µćc“¦·“Ó¦“ļµ½Ę½ŗā
C£®µćd(t1Ź±æĢ)ŗĶµće(t2Ź±æĢ)“¦n(N2)²»Ņ»Ńł
D£®ĘäĖūĢõ¼ž²»±ä£¬773 KĻĀ·“Ó¦ÖĮt1Ź±æĢ£¬n(H2)±ČÉĻĶ¼ÖŠdµćµÄÖµ“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĶ¼Ļń±ķ“ļÕżČ·µÄŹĒ

A. Ķ¼¢Ł±ķŹ¾25”ꏱ£¬ŗĶ0.1mol·L£1ŃĪĖįµĪ¶Ø20mL 0.1mol·L£1NaOHČÜŅŗ
B. Ķ¼¢Ś±ķŹ¾³£ĪĀĻĀ£¬µČĮæŠæ·ŪÓė×ćĮæµÄµČĢå»żµČÅØ¶ČµÄŃĪĖį·“Ó¦
C. Ķ¼¢Ū±ķŹ¾ĻņCaCl2ŗĶŃĪĖįµÄ»ģŗĻČÜŅŗÖŠµĪ¼ÓNa2CO3ČÜŅŗ
D. Ķ¼¢Ü±ķŹ¾ĻņŃĪĖįŗĶ“×Ėį»ģŗĻČÜŅŗÖŠµĪČė°±Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ņ»¶ØĢõ¼žĻĀ“ęŌŚ·“Ó¦C(s)+H2O(g)  CO(g)+H2(g)£ŗĻņ¼×”¢ŅŅ”¢±ūČżøöŗćČŻČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæCŗĶH2O£¬ø÷ČŻĘ÷ÖŠĪĀ¶Č”¢·“Ó¦ĪļµÄĘšŹ¼ĮæČēĻĀ±ķ£¬·“Ó¦¹ż³ĢÖŠCOµÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
CO(g)+H2(g)£ŗĻņ¼×”¢ŅŅ”¢±ūČżøöŗćČŻČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæCŗĶH2O£¬ø÷ČŻĘ÷ÖŠĪĀ¶Č”¢·“Ó¦ĪļµÄĘšŹ¼ĮæČēĻĀ±ķ£¬·“Ó¦¹ż³ĢÖŠCOµÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.¼×ČŻĘ÷ÖŠ£¬·“Ó¦ŌŚĒ°15 minµÄĘ½¾łĖŁĀŹv(H2)=0.1 mol·L£1·min£1
B.±ūČŻĘ÷µÄĢå»żV£¾0.5L C£®µ±ĪĀ¶ČĪŖT1 ”ꏱ£¬·“Ó¦µÄĘ½ŗā³£ŹżK=2.25
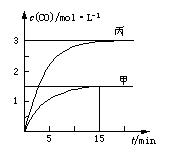 D£®ŅŅČŻĘ÷ÖŠ£¬ČōĘ½ŗāŹ±n(H2O)=0.4 mol£¬ŌņT1< T2
D£®ŅŅČŻĘ÷ÖŠ£¬ČōĘ½ŗāŹ±n(H2O)=0.4 mol£¬ŌņT1< T2
| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| ČŻ»ż | 0.5 L | 0.5 L | V |
| ĪĀ¶Č | T1 ”ę | T2 ”ę | T1 ”ę |
| ĘšŹ¼Įæ | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com