
| A. | 氨气液化以及液氨气化要吸热,所以氨常用于制冷剂 | |
| B. | 做红烧鱼时,常加一些食醋和料酒会更香,是因为生成少量的酯 | |
| C. | “地沟油”经过加工处理后可以用来制肥皂 | |
| D. | 利用生物方法脱除生活污水中的氮和磷,防止水体富营养化 |
分析 A、氨气的沸点高,易液化;
B、食醋和酒发生酯化反应生成有香味的酯类物质;
C、地沟油主要成分为高级脂肪酸甘油酯,碱性条件下水解为皂化反应;
D、氮和磷是植物的营养元素.
解答 解:A、氨气的沸点高,液化放热后气化吸热,则液氨气化吸收大量的热,所以液氨常用作制冷剂,故A错误;
B、食醋和酒发生酯化反应生成有香味的酯类物质,则红烧鱼更香,故B正确;
C、地沟油主要成分为高级脂肪酸甘油酯,碱性条件下水解生成高级脂肪酸盐,即为肥皂的主要成分,故C正确;
D、氮和磷是植物的营养元素,可造成水体富营养化,故D正确;
故选A.
点评 本题考查了氨气性质分析,酯化反应、酯的水解,注意化学知识的积累,掌握基础是解题关键,题目较简单.


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是表示化学反应快慢的物理量 | |
| B. | 一般情况下,升高温度能加快化学反应速率 | |
| C. | 可逆反应达到化学反应限度时,反应就静止不动了 | |
| D. | 可逆反应达到化学反应限度时,正反应速率等于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O2是${\;}_{8}^{16}$O2的同分异构体 | |
| B. | ${\;}_{8}^{18}$O2是O3的一种同素异形体 | |
| C. | ${\;}_{8}^{18}$O2与${\;}_{8}^{16}$O2互为同位素 | |
| D. | 1mol ${\;}_{8}^{18}$O2分子中含有20mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
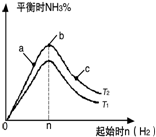 在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;
在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
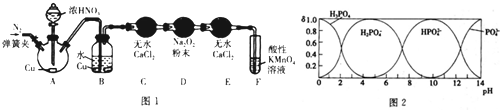
| 化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×108 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “地沟油”可以生产“生物燃料”,生物燃料本质上能量来源于太阳能 | |
| B. | 消除水体中的HgCl2污染可利用微生物使其转化为有机汞CH3HgCl | |
| C. | 人体内没有能使纤维素水解成葡萄糖的酶,但可以加强胃肠蠕动,有助于消化,因此纤维素是人类的营养食物 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是经提纯的二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN) | |
| B. | a mol•L-1HCN溶液与b mol•L-1NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于或等于b | |
| C. | HCN与Na2S溶液一定不能发生反应 | |
| D. | NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
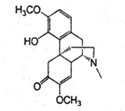
| A. | 每个青藤碱分子中含有2个手性碳原子 | |
| B. | 1mol最多能与1molBr2发生反应 | |
| C. | 1mol最多能与4molH2发生反应 | |
| D. | 青藤碱既能与盐酸反应又能与NaOH溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com