
Ⅰ.某校化学课外活动小组进行测定果汁中维生素C(分子式是C6H8O6)含量实验,下面是他们的实验过程及分析报告,请根据此报告填写有关空白。
(1)实验目的:测定××牌软包装鲜橙汁维生素C含量。
(2)实验原理:C6H8O6+I2→C6H6O6+2H++2I-
(3)实验用品和试剂:
①仪器和用品(自选,略)
②试剂:浓度为7.50×10-3mol?L-1的标准碘(水)溶液,指示剂,蒸馏水等。
(4)实验过程:
①洗涤仪器,检查是否漏液,用标准液润洗后装好标准液待用。在此步操作中,用标准液润洗的仪器是______________________。
②打开橙汁包,目测:颜色―橙黄色,澄清度―好,将酸式滴定管用橙汁润洗2~3遍,移取20.00mL橙汁入锥形瓶,向瓶中加入2滴指示剂,该指示剂的名称是___________________________。
③用左手操作滴定管,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化。滴定至终点时的现象是
___________________________________________________________________。
(5)数据记录和处理:(设计出表格,将三次滴定所得数据都填入表格中),若经数据处理,滴定中消耗标准碘溶液体积平均值为20.00mL,则此橙汁中维生素C的含量是__________________mg·L-1。
(6)记录测定结果时,滴定前仰视刻度线,滴定到达终点时又俯视刻度线,将导致滴定结果
_________________。(填“偏高”“偏低”或“无影响”)。
Ⅱ.某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的开关K时,观察到电流计的指针发生了偏转。
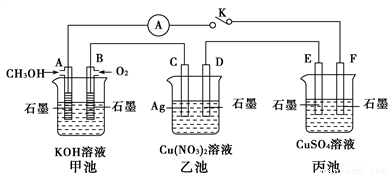
请回答下列问题:
(1)甲池为__________(填“原电池”“电解池”),A电极的电极反应式为_________________________
(2)丙池中F电极为_____________(填“正极”“负极”“阴极”或“阳极”),该池的总反应方程式为
____________________________________________________________
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_________mL(标准状况)。
(4)一段时间后,断开开关K。下列物质能使乙池恢复到反应前浓度的是_________(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2016-2017学年湖北省高二3月月考化学试卷(解析版) 题型:推断题
利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知:
请回答:
(1)写出下列反应方程式
①B+D→E______。
②G→H______。
(2)②的反应类型为______;F的官能团名称为______。
(3)E、J有多种同分异构体,符合下列条件的同分异构体有______种:
①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
写出其中酸催化水解产物能与FeCl3溶液发生显色反应的结构简式______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
下列反应产生的气体,通入Na2SO3溶液不反应的是
①Na2O2和CO2 ②Al和NaOH溶液 ③MnO2和浓盐酸共热
④浓硝酸和铜片 ⑤铜片和浓硫酸共热
A. ② B. ①② C.①②⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
常温下,向20mL的某稀H2SO4溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是
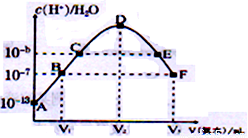
A. 稀硫酸的初始浓度为0.1mol/L B. V2=20mL
C. E溶液中存在:c(OH-)>c(H+) D. C点溶液pH=14-b
查看答案和解析>>
科目:高中化学 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
分子式为C4H10O,且不能与钠反应生成H2的结构有(不含立体异构)
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:选择题
现有X、Y、Z、W、Q五种短周期元素,原子序数依次增大,Y、Z、W、Q形成的简单离子具有相同的电子层结构,YX3、X2Z、X2Z2、W2Z、W2Z2都是常见的化合物,其中YX3在常温下呈气态,能使酚酞溶液变红色。下列有关推断正确的是( )
A. 简单离子半径:Q>W>Z>Y>X
B. YX3分子的VSEPR模型为四面体
C. X能分别与Y、Z、W形成共价化合物
D. Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:选择题
已知Ca(OH)2的饱和溶液中存在平衡:Ca(OH)2(s)  Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
A. 升高温度,平衡正向移动
B. 向溶液中加入少量碳酸钠粉末能增大钙离子浓度
C. 恒温下向溶液中加入CaO,溶液的pH不变
D. 向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高一3月月考化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:

(1)10种元素中,化学性质最不活泼的是________________。
(2)①、③、⑤三种元素最高价氧化物对应的水化物中,碱性最强的是___________。
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是____________。
(4)元素⑦的氢化物常温下和元素⑧的单质反应的化学方程式为:____________。
(5)①和⑨两种元素形成化合物的化学式为_________,该化合物溶液与元素⑧的单质反应的化学方程式为_______________。
(6)已知元素的电负性与元素的化合价一样,也是J已索的一种基本性质。下面给出14种元素的电负性。
元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
电负性 | 1.5 | 2 | 1.5 | 2.5 | 2.8 | 4 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,推测元素的电负性的变化规律是:_________,_________。
(2)预测Br与I元素电负性的大小关系_________,前四周期中,电负性最小的元素是_________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三“超级全能生”3月联考(选考科目)化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. C60与碳纳米管互为同素异形体
B. 最简式为CH3的有机物没有同分异构体
C. CH3C(CH3)2CH2CH3名称为2,2-二甲基丁烷
D. 核外电子总数和质子数均相同的微粒必为同种粒子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com